Meld je aan voor onze nieuwsbrief
Bij het aanmelden ga je akkoord met onze Privacy Policy
Veranderstrategie
Aanleidingen om te komen tot verandering in de organisatie kunnen in twee groepen worden verdeeld (2):
1. aanleidingen gericht op verbetering en vernieuwing, bijvoorbeeld omdat de organisatie de beste wil zijn, ambitie heeft, mogelijkheden ziet en kansen wil benutten;
2. aanleiding gericht op vermijden en verbeteren, bijvoorbeeld omdat er conflicten zijn, zwaarwegende problemen, onvrede, klachten en externe bedreigingen.
Beide soorten aanleidingen doen pijn, omdat vertrouwde paden verlaten moeten worden. Deze pijn is ook noodzakelijk, want zonder pijn is er geen urgentiebesef, geen probleemeigenaar en geen betrokkenheid en betrokkenheid is voorwaarde voor een goede oplossing.
John Kotter (1947), goeroe op het gebied van veranderingsmanagement en leiderschap, beschrijft in zijn boek: Onze ijsberg smelt (Kotter, 2006) (3), hoe een groep van keizerspinguïns komt tot een grote verandering: het verhuizen naar een andere ijsberg omdat hun eigen vertrouwde ijsberg niet meer te vertrouwen is: die smelt. Eén pinguïn ziet het gevaar, ziet dat er veranderd moet worden, maar hoe krijgt hij de groep zover dat alle pinguïns mee gaan met de vereiste verandering? Hoe krijgt hij draagvlak bij zijn medebewoners van de ijsberg? Kotter beschrijft in deze parabel aan de hand van zijn 8-stappenplan hoe de groep pinguïns het verandertraject doorloopt. Hieronder werk ik deze stappen, ook wel fasen genoemd, kort uit:
1. urgentiebesef vestigen;
2. de leidende coalitie vormen;
3. een visie en strategie ontwikkelen;
De eerste drie stappen hebben te maken met het besef dat de verandering noodzakelijk is. De pijnpunten moeten hier zichtbaar worden. In een organisatie zijn diverse factoren: specialisten, managers, verplegend personeel, die allemaal een eigen visie hebben op urgentie, visie en strategie. Verandering bewerkstelligen vanuit de werkvloer is goed, maar zonder steun van het management kom je er niet. Het is belangrijk om de verschillende perspectieven te herkennen en te erkennen en vanuit daar te komen tot een gedeelde urgentie: wat gaat er mis, waarom zal onze ijsberg smelten, we leven er al honderden jaren, niks aan de hand toch?
Fred is een pinguïn die heeft ontdekt dat de ijsberg, waar de groep pinguïns al jaren gelukkig en zorgeloos leeft, gaat smelten en binnenkort zou kunnen breken. Hij schrikt van zijn ontdekking en probeert de leiders ervan te overtuigen dat dit probleem speelt. Dit blijkt een politiek spel, waarbij lang niet alle leiders zich zomaar laten overtuigen. Fred laat zien waar de ijsberg smelt, onder het wateroppervlak namelijk, in een spleet, van binnenuit. Hij doet een praktijkdemonstratie, een simulatie, met een fles en zo zorgt hij dat hij medestanders krijgt en de vijf leiders, het topmanagement, overtuigt. Vervolgens wordt er gebrainstormd over ideeën, er komen allerlei oplossingsrichtingen voorbij. Dan kijkt een pinguïn naar boven en ziet een zeemeeuw vliegen….
In de leidende coalitie zitten mensen die aanzien hebben in de organisatie, qua geloofwaardigheid, deskundigheid en leiderschap. Die groep vormt een visie op de verandering en kijkt daarbij naar klanten, aandeelhouders, directie, medewerkers. Zo wordt begonnen met het creëren van een breed draagvlak voor de visie op de verandering en de gekozen strategie, wat essentieel is voor het slagen van het verandertraject. De nieuwe strategie van de pinguïns wordt, dat ze net als zeemeeuwen gaan trekken, ze worden een nomadenkolonie, die zich flexibel moet gaan opstellen. Verkenners worden erop uitgestuurd om nieuwe ijsbergen te ontdekken waar genoeg vis te vinden is en het ook goed toeven is.Nadat een breed besef voor de verandering is gegroeid, volgen de stappen 4,5 en 6:
4. de veranderingsvisie communiceren;
5. een breed draagvlak voor de verandering creëren;
6. korte-termijnsuccessen genereren.
De stappen 4, 5 en 6 zijn essentieel om de overige medewerkers bij het verandertraject te betrekken en daar komt het begrip weerstand (opnieuw) om de hoek. “Het gaat toch al jaren goed, waarom moet het dan opeens anders?”, “Dit is de zoveelste verandering in een paar jaar tijd: gedoemd te mislukken.” “De specialisten willen toch niet veranderen.” Met dit soort uitspraken dreigt dat het probleem in stand wordt gehouden en dat er niets verandert.
De groep pinguïns heeft geen zin om te verkassen, ze kennen die ijsberg van voor tot achter en weten dat daar goede vis in de buurt zit en dat het daar veilig is. De leidende coalitie start een campagne om de nieuwe nomaden life-style te promoten.
Draagvlak wordt gecreëerd onder de medewerkers door effectieve communicatie (eenvoudig, beeldspraken, herhalen, voorbeeldpersonen, twee richtingsverkeer), door te laten zien wat het effect is op de individuele medewerker, door een aantal passende interventies toe te passen en door te laten zien dat deze verandering het waard is. Alle pinguïns worden betrokken bij het veranderproces: er worden bijvoorbeeld verkenners gezocht die op zoek gaan naar geschikte leefplekken en bij terugkomst worden ze gelauwerd als helden.
7. verbeteringen consolideren en meer verandering tot stand brengen;
8. nieuwe benaderingen verankeren in de cultuur.
De laatste twee stappen dragen er zorg voor dat het verandertraject beklijft, dat veranderingen verankerd worden. Tips:
1. zorg voor een aantal “quick wins”, zinvolle successen die snel te realiseren zijn;
2. vier successen feestelijk;
3. visualiseer successen en behaalde resultaten;
4. blijf medewerkers betrekken, niet alles alleen willen doen als veranderaar, maar coalities zoeken.
De pinguïns passen langzaam tradities aan, cultuurveranderingen zijn bij pinguïns net zo weerbarstig als bij mensen… en in de loop der tijd worden steeds meer pinguïns tevreden over hun nieuwe stijl van leven: het nomadenbestaan.
Het stappenplan van Kotter is een vorm van geplande verandering, waarbij er bewust sturing wordt gegeven aan veranderingen, vaak topdown en waarbij het ontwerp is gescheiden van de uitvoering. Dit staat tegenover een ontwikkelgerichte benadering waarbij veranderingen veel meer worden gezien als een continue proces en waarbij samenwerking tussen mensen centraal staat. Kotter geeft aan dat zijn 8 stappen niet persé stap voor stap doorlopen moeten worden. Hij ziet het veranderen als een proces, waarbij je soms een fase teruggaat, of soms een aantal fasen combineert. Veel verandertrajecten gebruiken elementen van beide aanpakken. De keuze van het soort verandering is afhankelijk van diverse factoren, denk aan de aanleiding, urgentie (tijdsdruk), structuur en cultuur van de organisatie, niveau van de verandering (organisatie, groep of individu), veranderaar zelf. De ene benadering is niet beter dan de andere.
Van weerstand naar veranderbereidheid
Haast. Dat hebben veel topmanagers als er een verandering doorgevoerd moet worden. En door het rappe verandertempo wordt wel eens vergeten dat medewerkers weerstand kunnen vertonen en daarmee een negatieve invloed kunnen hebben op de verandering, doordat bijvoorbeeld het ziekteverzuim stijgt, het ‘roddelen’ toeneemt of de arbeidsproductiviteit afneemt. In elk verandertraject komt er in meer of mindere mate weerstand van medewerkers. Vier typische vormen van weerstand zijn aan te duiden als(4):
1. De saboteur speelt een actief politiek spel achter de schermen om tegenstanders te mobiliseren. Echter, dit doet hij achter de schermen, dus moeilijk grijpbaar;
2. De activist is heel volhardend en niet vatbaar voor argumenten, hij ventileert actief en openlijk waarom de verandering slecht is voor de organisatie;
3. De overlever zie je niet en hoor je niet bij een veranderproject. Deze medewerker past niet in de nieuwe organisatie, bijvoorbeeld door een vernieuwd competentieprofiel. Echter, dit heeft hij niet eens in de gaten. Deze mensen zijn niet zichtbaar, ze vallen niet op en worden daarom niet snel betrokken bij verandertrajecten. Het niets doen, het niet veranderen, blokkeert het verandertraject;
4. De zombie is zeer openlijk aanwezig en tegen de verandering: hij werkt immers al jaren op dezelfde wijze, geen noodzaak tot veranderen, toch? Waarom moeten we zo nodig veranderen? De zombie moppert graag en beïnvloedt zo op een negatieve wijze andere medewerkers.
Wat is het gevolg van deze vormen van weerstand? Weerstand heeft een negatieve klank. Volgens Metselaars en Cozijnsen(4) kun je weerstand beter positief benaderen. Weerstand is vaak ook een teken van betrokkenheid van medewerkers. Wellicht klopt een deel van de zorgen wel en kun je daar je voordeel mee halen. Weerstand wordt zo veranderbereidheid. De bereidheid tot veranderen hangt af van het kunnen, willen en moeten veranderen, waarbij het doel is dat uiteindelijk het gedrag verandert. Wie wil er niet enorm graag weer die drie kilo kwijt na de feestdagen, of 1 keer per week gaan sporten of eindelijk stoppen met roken (veranderbereidheid). Maar ja, vaak komt het er dan toch weer niet van (gedrag). Bij verandering gaat het daarom om gedragsverandering. Dit ligt hem in drie motivatoren: het moeten, willen en kunnen.
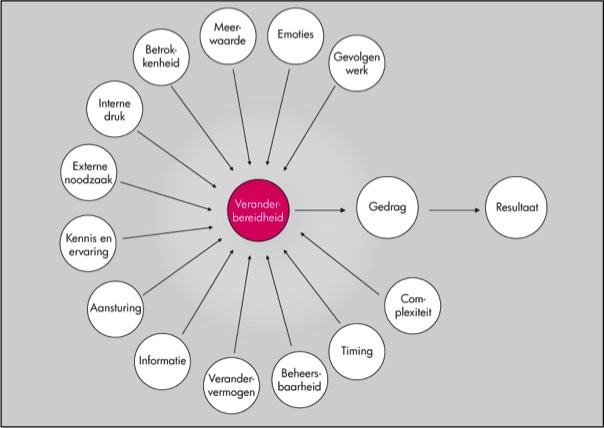
Willen de medewerkers wel veranderen: welke gevolgen worden er verwacht voor het werk, welke emoties roept het op, ziet men meerwaarde en wat is de betrokkenheid? Deze factoren wegen het zwaarst(4) en dat sluit aan op het stappenplan van Kotter, waarbij de urgentiebepaling als stap 1 staat. Wanneer mensen niet willen, blijft de veranderbereidheid laag.
Moeten medewerkers veranderen, oftewel, hoe staan de collega’s ertegenover en de directie, het management en de raad van bestuur. Dwingt de buitenwereld (bijvoorbeeld door technologische of politieke ontwikkelingen) tot verandering. Hoe sterk ervaart de medewerker de druk en de noodzaak? Wanneer de urgentie laag is, mensen weinig druk/ noodzaak zien, blijft de veranderbereidheid laag.
Kunnen medewerkers wel veranderen heeft te maken met de gedragcontrole die medewerkers ervaren. Hebben ze de juiste opleiding die nodig is bij de verandering, hoe wordt het veranderproces aangestuurd, hoe verloopt de communicatie, is de verandering te overzien? Samengevat: zijn er de juiste randvoorwaarden gecreëerd om de verandering mogelijk te maken? Zonder deze randvoorwaarden, blijft de veranderbereidheid laag en is het niet mogelijk om veranderingen te bewerkstelligen.
Metselaars en Cozijnsen(4) hebben een vragenlijst ontwikkeld (Dinamo-vragenlijst) waarmee de veranderbereidheid gemeten kan worden. Het is de bedoeling dat teamleiders of managers de vragenlijst van 44 vragen invullen en zo wordt dan het zogenaamde bereidheidsprofiel van het team in kaart gebracht. Vanuit daar wordt gekeken welke veranderstrategie ingezet kan worden en welke interventies op individueel, groeps- en organisatieniveau ingezet kunnen worden.
Ter illustratie de meerwaarde, een bouwsteen van het willen. Twee zorgorganisaties gaan fuseren, en de medewerkers zien geen meerwaarde van deze fusie. Dan is het goed om even stil te staan wat ook alweer het doel is van de verandering. Blijkbaar is dit niet bij alle betrokkenen helder. Een sleutelrol bij veel verandering is weggelegd voor het middenkader. Zij moeten vaak de veranderingen doorvertalen naar de werkvloer. Metselaars en Cozijnsen geven aan dat wanneer het doel van de verandering niet duidelijk is, in de veranderstrategie aandacht moet komen voor ‘overtuigen’, door in gesprek te gaan. De fusie is onomkeerbaar, medewerkers moeten overtuigd worden van de meerwaarde van de fusie. Op individueel niveau kan dit door bv leidende figuren aan te wijzen om de boodschap over te brengen, op groepsniveau kan er een sessie met het management worden georganiseerd en op organisatieniveau zal er een heldere visie ontwikkeld moeten worden. Zo geven Metselaars en Cozijnsen allerlei praktische handvaten voor interventies.
Tot slot
Er is niet één meest succesvolle veranderingbenadering. Er zijn diverse aanpakken mogelijk, waarbij het succes afhangt van vele factoren. Jeroen Busscher(1) heeft een paar algemene regels opgesteld: Verandertrajecten moeten..
1. leuk zijn en niet saai;
2. concreet zijn en niet te abstract;
3. behapbaar en klein zijn en niet te groot;
4. werken door groepsdruk en niet door regels.
En schrap het woord weerstand uit uw vocabulaire(2)!! Weerstand, of liever gezegd veranderbereidheid, geeft aan dat mensen betrokken zijn en op hun manier het beste willen voor zichzelf en voor de organisatie waar ze onderdeel van uitmaken. Door het gebruik van een vragenlijst en/of observatie kan een inschatting worden gemaakt van de veranderbereidheid en zo de motivatie achter de veranderbereidheid achterhaald worden. Dan kunnen de juiste interventies bepaald worden en neemt de kans van slagen van het verandertraject aanzienlijk toe. Medewerkers moeten serieus worden genomen, behandeld worden als individuen, met ieder eigen beweegredenen. De kunst van de veranderaar is om de veranderbereidheid serieus te nemen, en zo de energie van medewerkers te benutten. Want een verandertraject kan alleen maar slagen met betrokken en gemotiveerde medewerkers!
Literatuur
1. Busscher J. Pimp je afdeling! Academic Service, 2007.
2. Kleijn H F. Verandermanagement. Pearson, 2012.
3. Kotter J. Onze ijsberg smelt! Business Contact, 2006.
4. Metselaar E A. Van weerstand naar veranderbereidheid. Holland Business Publications, 2011.







