Meld je aan voor onze nieuwsbrief
Bij het aanmelden ga je akkoord met onze Privacy Policy
Inleiding
- Neurogeen hartfalen bij SAB berust niet op een myocard infarct. Het is een vorm van post-ischemische ?myocard stunning?.1,2,3,4
a. Het is niet veroorzaakt door op dat moment circulerende catecholamines.
b. Tijdens de zeer korte ictus ten tijde van het intracraniële aneurysma-ruptuur, komen overtollige catecholamines vrij (intracardiale catecholamines storm). De catecholamines komen rechtstreeks in het myocardium uit de synapsen van de ortho-sympathische zenuwuiteinden.
c. Het gevolg is ?calcium overload?, een mechanisme dat vergelijkbaar is met ?post-myocardial infarction myocardial stunning? en ?post cardiac surgery myocardial stunning?. Het hart is minder gevoelig geworden voor cellulaire calcium-instroom, waardoor de contractiliteit van het hart fors verminderd is. Dit kan echografisch aangetoond worden.
d. Bij proefdieren kan men neurogeen myocardfalen induceren nadat de bijnieren verwijderd zijn. Echter, neurogeen hartfalen kan niet ontstaan bij proefdieren met bijnieren nadat sympathectomie is uitgevoerd. Met andere woorden neurogeen hartfalen wordt niet veroorzaakt door circulerend catecholamines, maar door intracardiale catecholamines storm. 5
e. Het grootste deel van de wandbewegingsstoornissen wordt niet veroorzaakt door myocard infarct. Er zijn wel subendocardiale infarcten aanwezig, maar deze afwijkingen kunnen geen wandbewegingsstoornissen geven.
f. De contractiliteit is, zonder negatieve gevolgen voor het myocardium, door toediening van dobutamine, milrinone of levosimendan fors te verbeteren. Bovendien is de aandoening reversibel, de meeste patiënten hebben na 7 dagen geen echografische wandbewegingsstoornissen meer.
g. Ondanks dat er geen sprake is van een coronair bepaald myocard infarct, bestaat er toch hartweefselschade in het subendocardium. Dit is het grensgebied tussen endocardium en myocardium waar de perfusiedruk van het hart het laagst is. Dit gebied wordt ook wel het waterscheidingsgebied genoemd. - Daarnaast bestaat er een ischemische reactie van het centrale zenuwstelsel (CZS) van het type ?CUSHING? (zie: ?Bloeddrukregulatie bij intracraniële bloeding?, presentatie van Djo Hasan Venticare 2014).6
a. Acute en ernstige intracraniële druk (ICP)-verhoging kan leiden tot een zodanige afname van CBF waardoor cerebrale ischemie ontstaat. De vasoconstrictie en cardio-acceleratorneuronen in de vaso-motore centra (in de pons en medulla oblongata) worden onmiddellijk geactiveerd. Hierdoor nemen CO en systemische vaatweerstand toe waardoor hypertensie met hoge CO ontstaat. Door de hypertensie, worden baroreceptoren in de aortaboog geactiveerd. Dit leidt tot activatie van nervus Vagus en reactieve bradycardie.
b. Indien de CBF door deze maatregelen hersteld is, dan ontstaat er een nieuw evenwicht. Maar als de ICP heel hoog is kan dit leiden tot extreem hoge bloeddrukken. De bloeddruk kan zo hoog zijn dat er een zodanige afterload in het linker ventrikel ontstaat dat de hartpompfunctie niet toereikend is.
c. Door de hypertensie, worden baroreceptoren in de aortaboog geactiveerd. Dit leidt tot activatie van nervus Vagus en reactieve bradycardie.
Prevalentie
- Myocard dysfunctie
a. Systolische dysfunctie:
i. Segmentale wandbewegingsstoornissen bij opname 20%, na 8 dagen 29%, waaronder de volgende overlappende segmentale wandbewegingsstoornissen
1. Basale wandbewegingsstoornissen 14%
2. Midventriculaire wandbewegingsstoornissen 21%
3. Apicale wandbewegingsstoornissen 18%
ii. Het gebied van de wandbewegingsstoornissen kan niet verklaard worden vanuit het verzorgingsgebied van een coronaire arterie.
b. Diastolische dysfunctie bij 50.4% bij opname en bij 100% na 8 dagen.
2. ECG afwijkingen
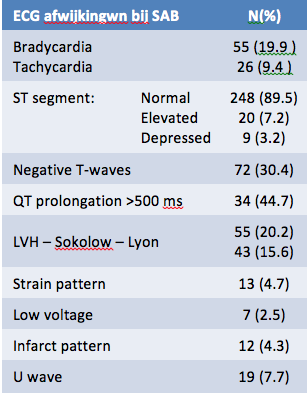
Klinische gevolgen
- Myocard dysfunctie leidt tot een hogere mortaliteit bij patiënten met aneurysmatische SAB.4
- Bij de preventie en behandeling van cerebrale ischemie wordt vaak de ?triple-H? therapie toegepast: Hypertensie, hypervolume en hemodilutie.1,2
i. De gedachte is dat:
- De kunstmatige hypertensie de perfusiedruk van de cerebrale vaten zou verhogen;
- De hypervolemie de cardiac output zou verhogen;
- En de hemodilutie zou de cerebrale doorstroming verbeteren door lage viscositeit, door compensatoire cardiac output verhoging.
ii. In de praktijk zijn de resultaten van deze behandeling fors tegengevallen.
- De hypertensie geeft een hogere kans op cerebrale hemorragische infarcten.
- De Diastolische dysfunctie reageert goed op de hypervolemie. Maar de marge tussen ondervullen (bij hogere vullingsdruk van het linker ventrikel en het rechter ventrikel door diastolische dysfunctie) en overvullen is zeer klein. De systolische dysfunctie van het linker ventrikel zorg voor vochtcongestie in de longvaten met longoedeem als gevolg.
- De hypertensie zorgt er ook voor dat het falende linkerventrikel minder pompt.
- Om de zuurstoftransportcapaciteit van het bloed naar de hersenen te verbeteren, dient de cardiac output compensatoire verhoogd te worden. Echter het falend linker ventrikel kan de benodigde cardiac output toename bij hemodilutie niet opbrengen. Hierdoor veroorzaakt hemodilutie anemie zonder betere bloeddoorstroming, dit leidt tot zuurstof tekort voor de hersenen.
3. Myocard functie bij neurogeen hartfalen neemt verder af bij toediening van nimodipine. Dat wil zeggen dat een deel van de voordelen van de neuroprotectieve werking van nimodipine bij deze patiënten verloren raakt. Dit is vooral bij intraveneuze toediening van nimodipine het geval.
4. Toediening van magnesium leidt tot verminderde contractiliteit, vasodilatatie, brady-aritmie en hypotensie. Bij patiënten met neurogeen hartfalen kan dit effect cerebrale ischemie bevorderen.
Take home message
Bij de behandeling van SAB patiënten dient men de aanwezigheid van neurogeen hartfalen door middel van echografie vast te stellen. Naar aanleiding van het resultaat van deze echografie, kan men de behandeling van de SAB aanpassen om te voorkomen dat deze behandeling de cardiac performance verslechtert.
Literatuur
- Hasan D. Triple-H therapy in aneurysmal subarachnoid haemorrhage (Editorial). Neth J Crit Care 2008;12:208-209
- Hasan D, Van der Bilt IAC. Treat, but meanwhile do not harm. Neurogenic myocardial dysfunction and pulmonary oedema (Editorial). Neth J Crit Care 2009;13:175-177
- Van der Bilt IA, Hasan D, Vandertop WP, Wilde AA, Algra A, Visser FC, Rinkel GJ. Impact of cardiac complications on outcome after aneurysmal subarachnoid hemorrhage: a meta-analysis. Neurology 2009;72:635-642
- Van der Bilt I, Hasan D, van den Brink R, Cramer MJ, van der Jagt M, van Kooten F, Meertens J, van den Berg M, Groen R, Ten Cate F, Kamp O, Götte M, Horn J, Groeneveld J, Vandertop P, Algra A, Visser F, Wilde A, Rinkel G; SEASAH (Serial Echocardiography After Subarachnoid Hemorrhage) Investigators. Cardiac dysfunction after aneurysmal subarachnoid hemorrhage: Relationship with outcome. Neurology 2014;82:351-358
- Novitzky D, Wicomb WN, Cooper DK, Rose AG, Reichart B. Prevention of myocardial injury during brain death by total cardiac sympathectomy in the Chacma baboon. Ann Thorac Surg 1986;41:520-524
- Guyton AC, Hall JE. Nervous regulation of the circulation, and rapid control of arterial pressure. Chapter 18. In: Guyton AC, Hall JE (eds). Textbook of medical physiology (Eleventh edition). Philadelphia, Elsevier 2006: pp 204-215