Meld je aan voor onze nieuwsbrief
Bij het aanmelden ga je akkoord met onze Privacy Policy
In acuut LF ontwikkelt encefalopathie zich na 8-28 dagen na het begin van icterus. Deze groep heeft een hoge mortaliteit, een hoge incidentie van cerebraal oedeem, en ook een sterk verlengde prothrombine tijd. De subacute vorm van LF kenmerkt zich door de ontwikkeling van encefalopathie ongeveer 5-12 weken na het begin van icterus. Ook deze groep heeft een hoge mortaliteit, ondanks een lage incidentie van cerebraal oedeem en veel minder afwijkende prothrombine tijd(1,2). Kinderen met LF worden in dit korte overzicht niet besproken, maar hebben een eigen indeling met bijbehorende prognose, afhankelijk van etiologie, leeftijd en ontwikkeling van klinische symptomen. De oorzaken van acuut LF (ALF) zijn vooral virale infecties en medicijnen of drugs gebruik. Incidenties verschillen wereldwijd enorm: in de UK wordt 54% van de gevallen van ALF veroorzaakt door paracetamol intoxicatie en terwijl bijvoorbeeld in Frankrijk hepatitis B 45% en de USA seronegatieve hepatitis 39% van de gevallen veroorzaken. Bij hepatitis A komt sporadisch ALF voor (0,14 – 0,35% van alle ziekenhuisopnames in de UK, 0,4% in de USA). Desondanks is het de meest voorkomende virale oorzaak in de UK. Het risico voor het ontwikkelen van ALF bij hepatitis A neemt toe met de leeftijd. Hepatitis B heeft een ALF incidentie van ongeveer 1-4% van gehospitaliseerde patiënten en het risico is hoger bij met hepatitis D of ? virus co-infectie.
Hepatitis D wordt in 34-43% van patiënten met ALF door hepatitis B gevonden, vergeleken met slechts 4-19% in minder ernstige gevallen. ALF kan ook ontstaan in het kader van een spontane reactivatie van een chronische hepatitis B infectie, zichtbaar door een seroconversie van hepatitis B >e= antigeen (HBeAg) naar hepatitis B >e= antibody (HBeAb). Vrouwen hebben een hoger risico voor ALF ten gevolge van hepatitis B. Bij hepatitis C komt weinig ALF voor: in een studie bij ALF werd slechts in ongeveer 2% van alle patiënten hepatitis C gevonden. Post-transfusie hepatitis, dat vooral door hepatitis C wordt veroorzaakt, leidt vrijwel nooit tot ALF. Hepatitis E komt voor in Azië en Afrika en het risico voor ALF varieert van 0,6-2,8% in mannen en niet-zwangere vrouwen tot meer dan 20% tijdens de zwangerschap, vooral tijdens het laatste trimester. Van hepatitis F en G is nooit overtuigend aangetoond dat deze ALF kunnen veroorzaken. Van seronegatieve of non A-E hepatitis wordt aangenomen (de diagnose wordt gesteld door uitsluiting van andere oorzaken), dat dit de meest voorkomende virale oorzaak van ALF is in de westerse wereld (in de UK 56% van de gevallen), Het risico voor het ontwikkelen van ALF door seronegatieve hepatitis is 2,3-4,7% van opgenomen gevallen.
Zeldzamer oorzaken van ALF zijn infecties met herpes simplex 1 en 2, herpesvirus-6, varicella-zoster virus, Epstein-Barr virus en cytomegalie virus. Van de geneesmiddelen is ALF beschreven bij gebruik van paracetamol, halothaan, isoniazide/rifampicine, NSAID=s, sulfonamides, flutamide, natrium valproaat, carbamazepine en MMDA (ecstacy). Paracetamol is natuurlijk het meest bekend als oorzaak van ALF. Het is de meest voorkomende oorzaak van ALF in de UK, maar in de rest van Europa vrijwel niet. Hoewel vaak als suicide middel is ontstaat 8% van ALF in het kader van normaal gebruik, meestal door ondoordacht gebruik van grotere hoeveelheden of bij patiënten met enzym inductie door anti-epileptica of bij regelmatig alcohol gebruik. Na een overdosis paracetamol ontstaat overigens maar in 2-5% ALF. De mediane dosis daarbij is in de UK 40 gram (5-210 gr) en de mortaliteit is het hoogst >48 gram. Halothaan, in gebruik als algemeen anestheticum, veroorzaakt bij herhaalde blootstelling een sensitisering waardoor het risico op ALF toeneemt met het aantal exposities (hoewel ook gevallen zijn beschreven door enfluraan en isofluraan). Andere oorzaken van ALF zijn onder andere de acute leverinsufficiëntie bij zwangerschap, vooral bij primi gravida met een mannelijke foetus, typerend ontstaan in het laatste deel van de zwangerschap, in patiënten met Wilson=s (koperstapelingsziekte) en na eten van Amanita phalloides, een paddestoel en een oorzaak die veel voorkomt in Midden- en Oost-Europa. Acuut LF veroorzaakt naast lever problemen ook functieverlies van andere organen. Hepatische encefalopathie (HE) komt voor in verschillende gradatie van ernst bij alle gevallen van ALF. Graad 1 of 2 kenmerkt zich door verschillende mate van slaperigheid en desoriëntatie, maar patiënten kunnen makkelijk worden gewekt en reageren op aanspreken.
Toename van de verschijnselen en ontwikkeling van graad 3 kenmerkt zich door een korte periode van onrust en agitatie, waarna ernstige verwarring optreed en patiënten slechts met moeite reageren op simpele vragen. Bij graad 4 is sprake van diep coma, met soms nog enige respons op forse pijnprikkels. Bij paracetamolintoxicatie is meestal sprake van HE ontwikkeling binnen 3 of 4 dagen na inname, bij andere oorzaken van ALF is dit variabel. Ammoniak, phenolen, vetzuren, >middle-molecular weight substances= en mercaptanen zijn genoemd als oorzakelijke stoffen. Zij hebben een negatieve invloed op het metabolisme in neuronen, met name op de energie huishouding, en veroorzaken in meer of mindere mate verandering in de bloed-hersenbarrière. Ook GABA, de belangrijkste inhiberende neurotransmitter, verhoogd bij ALF, werd in onderzoek gevonden als oorzaak. Verhoogde intracraniële druk (ICP) treedt op als complicatie bij HE graad 4 bij hyperacuut LF in tot meer dan 70%, tot 55% bij patiënten met acuut LF en in minder dan 15% van de gevallen met subacuut LF. Vaak is sprake van hersenoedeem. Het is een belangrijke doodsoorzaak en indien ernstig een frequente reden om niet meer voor transplantatie in aanmerking te komen. Klinisch kenmerkt cerebraal oedeem zich naast bewustzijnsveranderingen door systemische hypertensie, hyperventilatie, abnormale pupilreflexen en uiteindelijk uitval van stamreflexen en -functies.
Papiloedeem wordt niet vaak gezien. Nierfalen komt voor tot 75% van de gevallen met HE graad 4 na een paracetamol intoxicatie en in ongeveer 30% van andere oorzaken van ALF. Paracetamol heeft een direct toxisch effect op de nier en nierfalen ontwikkelt zich dan ook meestal vroeg. De andere oorzaken van ALF geven meestal pas nierfalen als zich ook encefalopathie heeft ontwikkelt en kenmerkt zich door een fase van functioneel nierfalen (urine Na < 10 mmol/l, urine/plasma osmolariteit ratio > 1,1). Metabole afwijkingen zoals hypoglycaemie komen vaak voor. Hypoglycaemie verschijnselen kunnen bij ALF gemaskeerd voorkomen en regelmatige bloedglucose controle is dan ook nodig. Metabole acidose komt voor bij 30% na ALF door paracetamol intoxicatie en is geassocieerd met een hoge mortaliteit (>90% als de arteriële pH <7,30 vanaf de tweede dag na inname). Deze acidose ontwikkelt zich voorafgaand aan encefalopathie en is onafhankelijk van de nierfunctie. In slechts 5% van de andere oorzaken van ALF wordt een metabole acidose gevonden, meestal later in het ziekteproces, maar ook geassocieerd met een slechte >outcome=. Hemodynamische veranderingen in ALF vertonen gelijkenis met het >systemic inflammatory respons syndrome= (SIRS): een hyperdynamische circulatie met verhoogde >cardiac output= en verminderde perifere vaatweerstand. Vasodilatatie veroorzaakt lage bloeddruk en een relatieve hypovolemie. Bij voortgaande verslechtering ontstaat in toenemende mate hart falen, een veel voorkomende oorzaak voor overlijden bij ALF. Pulmonale complicaties komen voor bij 50% van ALF(3).
Hyperventilatie is een teken van verhoogde intracraniële druk, of treedt op als reactie op de ontstane metabole acidose. Als de ICP toeneemt kan de ademhalingsprikkel onderdrukt worden als teken van uitval van de hersenstam functies, maar meestal zullen patiënten dan al beademd worden. Aspiratie bij verminderd bewustzijn vormt een gevaar voor het ontwikkelen van luchtweginfecties. Non-cardiogeen pulmonaal oedeem kan optreden tot ongeveer 40% van de gevallen, waarvan in de helft ook sprake is van pneumonie.In ALF zijn de spiegels van fibrinogeen, prothrombine en factoren V, VII, IX en X verlaagd. De prothrombinetijd wordt veel gebruikt als maat voor de ernst van het leverfalen(4). Los van factoren die door de lever worden gesynthetiseerd zijn ook thrombocyten in functie en aantal aangetast bij ALF, mogelijk direct of in het kader van verhoogd verbruik in de perifere circulatie door een laag-gradige vorm van gedissemineerde intravasale stolling. Bloedingen komen voor tot meer dan 70% van patiënten met ALF, waarvan ernstig tot 30%.
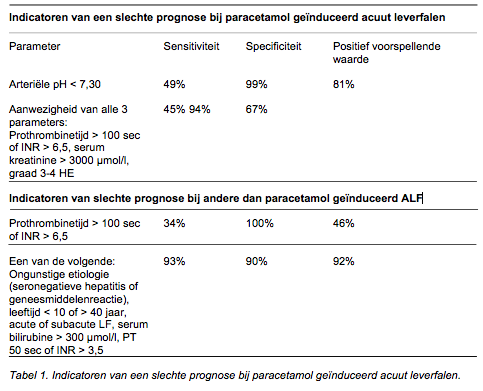
Meest gastrointestinaal, maar ook worden bloedingen gezien uit nasofarynx, longen, nieren, retroperitoneum en punctieplaatsen (centrale lijn, drains). Patiënten met ALF hebben een ongeveer 50% verhoogd risico voor infecties. Bij ALF is er een slechte correlatie tussen infectie en klinische verschijnselen zoals koorts, maar ook met lab uitslagen zoals aantal leucocyten. Bij ALF patiënten met HE graad 2 werden tot 80% bacteriële infecties, en meer dan 30% fungus infecties gevonden met positieve kweken van bloed, sputum, urine en van tipkweken van infuuslijnen. De fungus infecties werden in slechts 50% pre-mortaal vastgesteld. De prognose van ALF wordt, los van de etiologie, ingegeven door twee belangrijke kenmerken: de noodzaak om een patiënt over te plaatsen voor behandeling naar een specialistisch centrum en de indicatie voor een levertransplantatie. Door de grote variabiliteit in oorzaak kan niet goed een algemene prognose worden gegeven. Verschillende scoringsmethoden zijn in gebruik waarvan die van King=s College London(5) een van de meest gebruikte (Tabel 1).
Acute-on-chronic lever falen
Acute-on-chronic lever falen (ACLF) wordt gezien als een aparte entiteit waarbij sprake is van een acute achteruitgang van leverfunctie in patiënten met cirrhose, veroorzaakt door extrahepatische factoren zoals ernstige infecties met eind-orgaan dysfunctie tot gevolg, of een bijkomende leveraandoening zoals ischemie ten gevolge van een low flow status in het splanchnicus gebied, bijvoorbeeld door shock ten gevolge van een varices bloeding. Een enkele maal wordt geen oorzaak gevonden. Kenmerkend voor ACLF is de snelle progressie, de noodzaak voor ondersteuning van meerdere orgaansystemen en de hoge mortaliteit, die kan variëren van 50-90% op de korte en middellange termijn(6). Hoewel er controverse is over wat nu precies ACLF is, werd in een recent overzicht van Jalan(7) de geldende definitie voor ACLF aangehaald van EASL-AASLD(8): >Acute deterioration of pre-existing, chronic liver disease, usually related to a precipitating event and associated with increased mortality at 3 months due to multi-system organ failure.
De prognose van de patiënt met ACLF wordt bepaald door de ernst van het orgaan falen, niet door het oorspronkelijk lever probleem. Uit onderzoek blijkt ook dat de gehanteerde scoringssystemen voor het bepalen van de ernst van leverziekten zoals de Child-Pugh en de MELD-score minder goed discrimineren dan de bekende IC opname scores als SOFA en APACHE II(7). Verschillende oorzaken voor ACLF zijn aan te geven: trauma, een chirurgische ingreep, varices bloedingen of infecties kunnen aanleiding geven tot acute verslechtering van de leverfunctie bij patiënten met een bestaande cirrhose. Denk ook aan alcoholische hepatitis, drug-induced liver injury, bijkomende virale hepatitis, met name hepatitis A, thrombose van de vena portae en ischemische hepatitis. Infectie is een vaak voorkomende complicerende factor bij cirrhose patiënten. Ongeveer 40-50% van ziekenhuisopnames bij cirrhose is ten gevolge van sepsis en nog eens 20-40% ontwikkelt een nosocomiale infectie. De overall mortaliteit in het ziekenhuis van cirrhose patiënten met een infectie is ongeveer 15%, oplopend tot 60-100% bij een ernstige bacteriële infectie met septische shock(9).
De gevolgen van een infectie zijn toename van hepatische encefalopathie, renale dysfunctie en mortaliteit geassocieerd met varices bloeding. Door de relatie tussen infectie en SIRS bij het ontstaan van de complicaties bij cirrhose wordt dan ook gedacht dat een inflammatoire reactie leidt tot een gestoorde immuunrespons waardoor cirrhose patiënten een vergrote kans hebben op infecties. Ook genetische factoren spelen een rol: bij cirrhose patiënten met een variant in hun TLR2 receptor, betrokken bij de reactie op infectie, was het risico voor spontane bacteriële peritonitis (SPB) bijvoorbeeld sterk verhoogd(10). Bij alcoholische hepatitis werd een verminderde fagocyterende functie van neutrofielen aangetoond, met als gevolg een verhoogd risico voor infectie, orgaan falen en verhoogde mortaliteit(11). Bij ACLF zijn hyperbilirubinaemie en coagulopathie de belangrijkste kenmerken van progressief leverfalen. Bilirubinostasis is niet alleen vroeg teken van achteruitgang van de leverfunctie, maar ook geassocieerd met een verhoogd risico op infectie. Inflammatie van de lever is een determinant van portale hypertensie en prognose in cirrhose. Patiënten met een alcoholische hepatitis en ACLF hebben een verhoogd plasma TNF-?, geassocieerd met hogere portale druk. Endotoxine vanuit de darm speelt ook een rol bij portale hypertensie. Vermindering van de bacteriële >load= door gebruik van antibiotica als quinolonen en riampicine leidde tot een reductie van inflammatie en portale druk(7). De microcirculatie in de lever bij cirrhose wordt bedreigd door een afname in de eNOS activiteit, waardoor minder productie van vasodilatatoir NO mogelijk is(12). Hoewel het hepatorenale syndroom (HRS) met vasodilatite in het splanchnicus gebied, verlaagde arteriële bloeddruk, sterke renale vasoconstrictie, verminderde cardiale funtie en activatie van sympathicus en verschillende neurohormonale systemen optreedt, kan het bij ACLF sterk variëren.
Bij sommige patiënten is vooral sprake van circulatoire veranderingen terwijl bij anderen een verhoogde vorming van pro-inflammatoire mediatoren op de voorgrond staat. Toediening van terlipressine en albumine als standaard therapie bij HRS worden gebruikt, maar zijn niet succesvol bij 54% van ACLF(13). Gedacht wordt dat ook hier de ontsteking bij ACLF het verschil veroorzaakt. Albumine heeft wel een beschermend effect op de nierfunctie bij SPB, ondanks het bovenstaande. De ontwikkeling van hepatische encefalopathie met zwelling van het brein wordt bij ACLF net als bij acuut leverfalen gevonden. Verhoogde intracraniële druk is in verschillende studies aangetoond. Ammoniak speelt een belangrijke rol, maar een relatie tussen een bepaalde plasma spiegel en de ernst van HE is niet zo duidelijk. Wel lijkt er een synergisme tussen ammoniak en ontsteking te zijn, waarbij in proefdiermodellen ammoniak het brein als het ware >primed= en gevoeliger maakt voor een bijkomende infectie en de gevolgen daarvan, en vermindering van ammoniak of vermindering van bacteriële translocatie door preventief gebruik van antibiotica bescherming geeft.
Afkortingen
ACLF acute-on-chronic lever falen
ALF acuut lever falen
APACHE II Acute Physiology, Age and Chronic Health Evaluation (score)
HE hepatische encefalopathie
ICP intracraniële druk
LF lever falen
MELD Model of End Stage Liver Disease (score)
SOFAS equential Organ Failure (score)
Literatuur
1. O’Grady JG. Acute Liver Failure. In: Comprehensive Clinical Hepatology. Edited by O’Grady JG, Lake JR, Howdle PD, vol. 1, 1 edn. London: Harcourt Publishers; 2000: 30.01-30.20.
2. O’Grady JG, Schalm SW, Williams R. Acute liver failure: redefining the syndromes. Lancet 1993;342(8866):273-275.
3. Baudouin SV, Howdle P, O’Grady JG, Webster NR. Acute lung injury in fulminant hepatic failure following paracetamol poisoning. Thorax 1995;50(4):399-402.
4. Harrison PM, O’Grady JG, Keays RT, Alexander GJ, Williams R. Serial prothrombin time as prognostic indicator in paracetamol induced fulminant hepatic failure. BMJ 1990;301(6758):964-966.
5. O’Grady JG, Alexander GJ, Hayllar KM, Williams R. Early indicators of prognosis in fulminant hepatic failure. Gastroenterology 1989;97(2):439-445.
6. Jalan R, Williams R. Acute-on-chronic liver failure: pathophysiological basis of therapeutic options. Blood purification 2002;20(3):252-261.
7. Jalan R, Gines P, Olson JC, Mookerjee RP, Moreau R, Garcia-Tsao G, Arroyo V, Kamath PS. Acute-on chronic liver failure. J Hepatol 2012;57(6):1336-1348.
8. Olson JC, Wendon JA, Kramer DJ, Arroyo V, Jalan R, Garcia-Tsao G, Kamath PS. Intensive care of the patient with cirrhosis. Hepatology 2011;54(5):1864-1872.
9. Arvaniti V, D’Amico G, Fede G, Manousou P, Tsochatzis E, Pleguezuelo M, Burroughs AK. Infections in patients with cirrhosis increase mortality four-fold and should be used in determining prognosis. Gastroenterology 2010;139(4):1246-1256, 1256 e1241-1245.
10. Nischalke HD, Berger C, Aldenhoff K, Thyssen L, Gentemann M, Grunhage F, Lammert F, Nattermann J, Sauerbruch T, Spengler U et al. Toll-like receptor (TLR) 2 promoter and intron 2 polymorphisms are associated with increased risk for spontaneous bacterial peritonitis in liver cirrhosis. J Hepatol 2011;55(5):1010-1016.
11. Mookerjee RP, Stadlbauer V, Lidder S, Wright GA, Hodges SJ, Davies NA, Jalan R. Neutrophil dysfunction in alcoholic hepatitis superimposed on cirrhosis is reversible and predicts the outcome. Hepatology 2007;46(3):831-840.
12. Mookerjee RP, Malaki M, Davies NA, Hodges SJ, Dalton RN, Turner C, Sen S, Williams R, Leiper J, Vallance P et al. Increasing dimethylarginine levels are associated with adverse clinical outcome in severe alcoholic hepatitis. Hepatology 2007;45(1):62-71.
13. Martin-Llahi M, Guevara M, Torre A, Fagundes C, Restuccia T, Gilabert R, Sola E, Pereira G, Marinelli M, Pavesi M et al. Prognostic importance of the cause of renal failure in patients with cirrhosis. Gastroenterology 2011;140(2):488-496 e484.






