Meld je aan voor onze nieuwsbrief
Bij het aanmelden ga je akkoord met onze Privacy Policy
Verschijnselen van het Guillain-Barré syndroom
Verschijnselen van het Guillain-Barré syndroom (GBS) ontstaan doordat de zenuwen beschadigd raken en daardoor de elektrische impulsen slecht of helemaal niet geleiden. Hierdoor ontstaan de verlammingsverschijnselen; het meest in het oog springende symptoom van het GBS. Deze verlammingen ontstaan in uren tot dagen en het dieptepunt wordt per definitie binnen vier weken bereikt. Bij het merendeel van de patiënten wordt het dieptepunt echter al binnen twee weken bereikt. Meestal begint de zwakte in de benen. De ernst van de zwakte is zeer verschillend van patiënt tot patiënt; sommige patiënten hebben op het dieptepunt van de ziekte mild krachtsverlies en blijven in staat zelfstandig te lopen, terwijl andere patiënten volledig verlamd raken. Twintig tot dertig procent van de patiënten raakt respiratoir insufficiënt(3), dit is meestal het gevolg van zwakte van de ademhalingsspieren, met inbegrip van het diafragma en de intercostaal spieren. In enkele uren kan er soms al een forse toename van zwakte van de ademhalingsspieren zijn. Om die reden moeten patiënten in de progressieve fase van de ziekte zeer goed gemonitord worden. Het is van belang de ademfrequentie te controleren en te kijken of de patiënt zijn hulpademhalingsspieren gebruikt. Een test om de respiratoire zwakte te meten is de patiënt herhaaldelijk vragen zover mogelijk hardop te tellen in een ademteug. Een andere test is het herhaaldelijk meten van de vitale capaciteit, deze meting is echter alleen goed mogelijk wanneer er geen aangezichtszwakte bestaat. In het algemeen lopen de bloedgaswaarden en de zuurstofsaturatie achter bij deze parameters en moeten afwijkende waarden beschouwd worden als late tekenen van dreigende respiratoire insufficiëntie. Herhaaldelijke CO2-metingen in de bloedgas kunnen wel waardevol zijn om beginnende respiratoire insufficiëntie vast te stellen. Recent is er een model gemaakt waarmee bij opname in het ziekenhuis nauwkeurig voorspeld kan worden hoe groot de kans is dat de patiënt aan de beademing zal komen. De kans op beademing wordt groter als de patiënt een snelle ziekte progressie heeft, ernstige zwakte heeft en aangezichtszwakte en/of zwakte van de slikspieren heeft(4). Aan de hand van deze parameters kan eenvoudig een score bepaald worden (Erasmus GBS Respiratoire Insufficiëntie Score; EGRIS), waarbij een bepaalde kans op beademing hoort. Meer dan de helft van de Guillain-Barré patiënten heeft een gestoorde sensibiliteit. Patiënten klagen over een doof en afwijkend gevoel in armen en benen. Meestal beginnen deze klachten in de handen en voeten en trekken omhoog richting de romp. Samen met de spierzwakte zorgt het gestoorde gevoel ervoor dat Guillain-Barré patiënten in zeer korte tijd ernstig ge- handicapt raken. De aangezichtszenuwen zijn vaak bij het proces betrokken en kunnen een dubbelzijdige aangezichtsverlamming veroorzaken. Hierbij is het belangrijk te letten op een goede oogsluiting om cornea beschadiging te voorkomen. De spieren die bij het slikken betrokken zijn kunnen ook aangedaan zijn en het is belangrijk hierop te letten om verslikken te voorkomen. Soms hebben patiënten last van dubbelzien, dit ontstaat als de oogspieren bij de ziekte betrokken zijn.
Pijn is een ernstig en veelvoorkomend symptoom(5). Pijn is ook vaak een presenterende klacht, nog voordat de zwakte ontstaat. Dit kan voor diagnostische problemen zorgen. Herkenning van deze klacht is erg belangrijk, vooral bij patiënten die slecht kunnen communiceren omdat ze beademd worden. Autonome disfunctie is een complicatie van het GBS, die bij ongeveer de helft van de patiënten voorkomt. Dit kan resulteren in diverse symptomen zoals verschillende typen van cardiale ritme stoornissen, bloeddruk fluctuaties, abnormale hemodynamische fluctuaties op medicatie, overmatig zweten, pupilafwijkingen, blaasdisfunctie en darmdisfunctie(6). Hierdoor kunnen er ook levensbedreigende cardiovasculaire complicaties ontstaan. Drie tot tien procent van de Guillain-Barré patiënten overlijdt aan de ziekte. Oorzaken hiervan zijn een pneumonie, sepsis, het adult respiratory distress syndrome of longembolieën(7). In zeldzame gevallen is plotse hartdood ten gevolge van autonome disfunctie de oorzaak. Guillain-Barré patiënten ervaren vaak ernstige vermoeidheid en dit symptoom blijft in vele gevallen tot jaren na ontstaan van de ziekte bestaan ook nadat de neurologische uitvalsverschijnselen zijn verdwenen(8-9). Hierdoor is het een vervelend en invaliderend symptoom wat de laatste jaren terecht meer aandacht heeft gekregen. Over het algemeen is het voorkomen van vermoeidheid bij Guillain-Barré patiënten niet afhankelijk van de uitgebreidheid van de (resterende) neurologische symptomen(10). Met een trainingsprogramma zijn de vermoeidheidsklachten gunstig te beïnvloeden(11). Het GBS tast het bewustzijn en de cognitieve functies niet aan. Het is dus belangrijk om voor ogen te houden dat de Guillain-Barré patiënt vaak zeer moeizaam kan communiceren door de verlamming en door de endotracheale beademing, maar wel kan horen, zien, voelen en denken. Hierin verschillen Guillain-Barré patiënten van andere patiënten opgenomen op de Intensive Care. Guillain-Barré patiënten vragen om een speciale benadering van medisch en verplegend personeel, waarbij men steeds in gedachte moet houden dat ondanks het onvermogen zich uit te drukken, ze wel alles horen, pijn kunnen voelen en radeloos kunnen zijn.
Het beloop
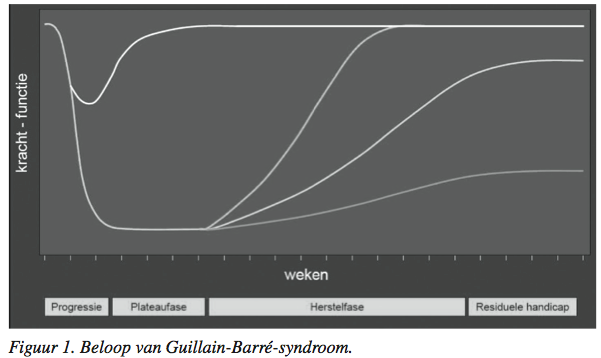
De meeste patiënten bereiken binnen twee weken het dieptepunt van hun klachten en per definitie moet het dieptepunt binnen vier weken bereikt zijn. Patiënten blijven gedurende dagen tot weken op het dieptepunt van de klachten, dit wordt de plateaufase van de ziekte genoemd. Na deze plateaufase treedt langzaam herstel op. Dit herstel kan weken tot maanden duren. Niet alle patiënten herstellen restloos van de ziekte. Twintig procent van de ernstig aangedane patiënten kan na zes maanden nog niet zelfstandig lopen(12) en ongeveer een derde heeft na 1-2 jaar nog problemen met lopen en is nog niet in staat om te werken(13). Drie tot zes jaar na ontstaan van de ziekte rapporteert ongeveer 60% van de Guillain-Barré patiënten veranderingen in hun levensstijl, werk en vrijetijdsbesteding. Dit geldt ook voor hun partners. De veranderingen worden veroorzaakt door lichamelijke beperkingen, verminderde conditie en vermoeidheid(14-15). Het verloop van de ziekte is zeer heterogeen (zie figuur 1). Ongeveer 10% van de Guillain-Barré-patiënten gaat na een aanvankelijke verbetering of stabilisatie één tot meerdere keren achteruit. Dit treedt meestal op binnen 9 weken(16).
Behandeling
De belangrijkste hoeksteen voor de behandeling bij het GBS is ondersteunende zorg. Een multidisciplinair beleid is van belang voor de behandeling het voorkomen van mogelijke complicaties zo- als respiratoire insufficiëntie, autonome disfunctie waaronder ileus en urineretentie en diepe veneuze trombose. Bewaking op een de Intensive Care is geïndiceerd bij snel progressieve spierzwakte, autonome disfunctie en (dreigende) respiratoire insufficiëntie. Het op de voorgrond staan van spraak- en slikstoornissen zijn belangrijke risicofactoren voor het ontstaan van respiratoire insufficiëntie en kan een reden zijn om preventieve bewaking op een intensive care in te stellen. In dit kader is het nut- tig een EGRIS score af te nemen om daarmee de kans op beademing te voorspellen (zie eerder). De voorkeursbehandeling met medicamenten bestaat uit het geven van intraveneuze gammaglobulines (IVIg) in een dosering van 0,4 gram per kg lichaamsgewicht per dag gedurende 5 dagen. Even effectief maar invasiever en hogere kans op complicaties is plasmaferese. De behandeling met IVIg verkort effectief de ziekteduur. De tijd nodig voor een patiënt om weer zelfstandig te kunnen lopen wordt ongeveer gehalveerd met deze behandeling. Patiënten lopen gemiddeld 1 maand eerder wanneer zij behandeld worden en hebben een betere uitkomst na 1 jaar(17). Corticosteroïden als monotherapie bleken niet effectief en kan bij Guillain-Barré patiënten met een puur motore uitval zelfs verslechtering uitlokken(18). Toevoeging van methylprednisolon aan een IVIg kuur heeft geen toegevoegde waarde op het uiteindelijk herstel, maar is mogelijk net wat effectiever op de korte termijn(19). Het is niet aangetoond dat het zinvol is om patiënten eerst IVIg te geven en bij uitblijven van herstel plasmaferese te proberen(20). Het wordt momenteel uitgezocht of het zinvol is om bij uitblijven van herstel een tweede kuur IVIg te geven. Patiënten die aanvankelijk verbeteren na IVIg en na stoppen van de therapie opnieuw verslechteren, moeten opnieuw met IVIg worden behandeld. Relevante bijwerkingen van IVIg zijn anafylactische reacties, nefrotoxiciteit, hemolytische anemie, aseptische meningitis en het thrombo-embolische complicaties, zoals TIA?s. Een contra-indicatie is het bestaan van een bekende selectieve IgA deficiëntie. Verder treden bij IVIg behandeling frequent voorbijgaande bijwerkingen op zoals koorts, hoofdpijn, duizeligheid, rillingen en urticaria welke vermoedelijk gerelateerd zijn aan interleukines aanwezig in het IVIg preparaat. Deze voorbijgaande bijwerkingen kunnen voorkomen worden door de infuussnelheid te verlagen.
Pathogenese
Het GBS ontstaat in tweederde van de gevallen enkele dagen tot maximaal vier weken na een infectie. Bovenste luchtweginfecties en gastroenteritis vormen de belangrijkste vormen van infectie. De meest gevonden verwekkers zijn Campylobacter jejuni, Heamophilus Influenza, CMV, EBV en Mycoplasma pneumoniae(21). Deze infecties veroorzaken een immunologische kruisreactie waarbij antistoffen worden gevormd die binden aan structuren aanwezig op de celmembraan van perifere zenuwen. De structuren waar de antistoffen aan binden vertonen grote gelijkenis met oppervlakte moleculen op bacteriën die GBS kunnen uitlokken zoals C. jejuni en H. Influenza. Vermoedelijk brengen deze bacteriën dit soort moleculen tot expressie om het immuunsysteem van de geïnfecteerde gastheer te misleiden. Dit wordt ook wel ?moleculaire mimicry? genoemd. Bij GBS leidt dit tot een ontsporing van de immuunreactie en de vorming van antistoffen gericht tegen het eigen zenuwstelsel(22). Hoe het komt dat niet iedereen GBS krijgt na een dergelijke infectie en wat het onderliggende mechanisme bij patiënten met andere infecties is, wordt momenteel nog onderzocht. Vermoedelijk spelen hierbij zowel factoren bij de patiënt, zoals een erfelijk bepaal- de verhoogde vatbaarheid, als pathogene factoren, zoals het tot expressie brengen van neurale structuren op bacteriën en virussen, een rol. Het GBS is geen besmettelijke of erfelijke ziekte. Mogelijk hebben bepaalde mensen wel een wat verhoogde kans om de ziekte te krijgen. Onderzoek is noodzakelijk om dit verder uit te zoeken.
De Guillain-Barré patiënt op de Intensive Care
De patiënt met Guillain-Barré kan een indrukwekkend beeld geven. Een veelal voorheen gezond persoon wordt in zeer korte tijd getroffen door ernstige uitvalsverschijnselen, welke hem of haar in grote mate afhankelijk maken van de zorgverlening. Dit roept vaak heftige reacties van de patiënt en zijn of haar omgeving op. Dit vraagt van verpleging en behandelaars een grote betrokkenheid en speciaal inzicht in deze aandoening. Regelmatig zijn patiënten geheel verlamd en beademd en kunnen langere tijd (maanden) in deze toestand zijn totdat er herstel optreedt. Gemiddeld worden GBS-patiënten gedurende 4-5 weken beademd. De toestand van deze patiënten kan soms uitzichtloos lijken, voor de patiënt, maar ook voor de familie. Het is belangrijk om altijd voor ogen te houden dat veel van deze patiënten redelijk tot goed herstellen. Aan het begin van de ziekte is communicatie vaak nog mogelijk en dit moment moet worden aangegrepen om de patiënt uitleg te geven over de ziekte.
Ervaring GBS-patiënt: ?Ik denk nu, dat ik een groot gedeelte van mijn genezing te danken heb aan het feit, dat de neuroloog gezegd heeft dat het voor 100% te genezen valt en dat dat aldoor in mijn achterhoofd mee heeft gespeeld. Hij zegt tevens dat er met medicatie (immunoglobulinen) gestart gaat worden gedurende 5 dagen. Ook zegt hij dat ik de komende 5 dagen qua gezondheid nog wel achteruit zou gaan?. (Bron: www.guillainbarre.nl)
De Guillain-Barré patiënt op de Intensive Care zal zich vaak opgesloten, angstig en geïsoleerd voelen. Communicatie moet een grote prioriteit hebben bij deze patiënten. Het is goed om voor een klok en kalender te zorgen en proberen alternatieve manieren voor communicatie te vinden. Het is belangrijk goede vaste afspraken te maken en deze naast het bed van de patiënt te hangen, bijvoorbeeld dat een keer knipperen met de oogleden ?ja? betekend en twee keer ?nee?. Van groot belang is ook om een ernstig verlamde patiënt nooit alleen te laten zonder de patiënt een middel te geven waarmee hij of zij alarm kan slaan, bijvoorbeeld met een alarmbel die bediend kan worden met de mond.
Ervaring GBS-patiënt: ?Een van de ergste dingen vond ik, dat ik op geen enkele manier de verpleging kon ?roepen?. Ik kon geen bel indrukken, want ik kon me natuurlijk niet bewegen. En ik kon niet roepen. Dit was soms een beetje beangstigend, want je weet maar nooit waar je iemand voor nodig had. Op een gegeven moment hebben ze een blaasbel aangelegd, maar toen had ik nog geen kracht genoeg om te blazen. We probeer- den dat iedere dag en op een gegeven moment lukte het. Maar volgens mij lag ik toen al een dikke 2- 2,5 week zonder. Op een gegeven moment had ik door, dat als ik zelf niet mee ademde met het beademingsapparaat, er een alarm afging. Als ik dan iemand nodig had (en dat was meestal voor het wegzuigen van slijm, want daar kreeg ik het benauwd van), hield ik gewoon een tijdje op met zelf ademen, totdat het alarm afging. En dan kwam er iemand?. (Bron: www.guillainbarre.nl)
Veel patiënten met het GBS hebben pijn. Deze pijn kan ernstig zijn. Het is belangrijk om patiënten die geïntubeerd zijn en dus slecht kunnen communiceren te vragen of ze last van pijn hebben. Deze pijn kan dan behandeld worden met pijnstillers volgens de WHO- pijnladder of als er sprake is van neuropathische pijn, met antidepressiva (amitriptyline) of anti-epileptica. Als patiënten behandeld worden voor pijn is het belangrijk het effect van die behandeling regelmatig te blijven monitoren. Het van belang in een vroeg stadium de fysiotherapeut en de revalidatiearts in consult te vragen. Dit om klachten van spierstijfheid, contracturen en spitsvoeten te voorkomen en om plannen te maken voor de toekomst.
Ervaring GBS-patiënt: ?Dat ik pijn had, wisten ze niet, want ik kon het niet kenbaar maken. Als ze me dan kwamen zeggen dat ze me gingen draaien, kon ik heel voorzichtig nee schudden. Maar waarom, dat wisten ze niet. Vreselijke pijn heb ik dan gehad. Als ik eenmaal op mijn zij lag, vroegen ze, of ik goed lag. Nee dus. Dan gingen ze wat rommelen met kussens, maar nog steeds nee dus. Ze begrepen dus wel, dat ik niet lekker lag. Nou zeiden ze, je hoeft maar een uurtje. En dat was dus niet vol te houden. Uiteindelijk had een verpleegster op een gegeven moment door dat ik pijn had. Ze vroeg het me en ik knikte zo hard ik kon ja. Er werd toen besloten dat ik wel op mijn zij moest af en toe, maar niet langer dan een half uurtje?! (Bron: www.guillain-barre.nl)
Het is belangrijk te zorgen dat patiënten het realiteitsbesef niet kwijt raken. Een aantal maatregelen om dit te bereiken zijn: een klok met 24- uurs aanduiding binnen gezichtsbereik, ruime bezoekuren voor familieleden en naasten, zoveel mogelijk bewaren van het dagnachtritme en voorkomen van over- of onderprikkeling. Radio, tv en luisterboeken kunnen heel waardevol zijn. Tijdens deze fase van de ziekte is het ook belangrijk de patiënt steeds te blijven betrekken bij beslissingen. Ook kleine beslissingen, bijvoorbeeld of het licht aan of uit moet. En ook al kan de patiënt niet terugpraten, niet over de patiënt spreken in zijn of haar bijzijn en handelingen uitleggen en aankondigen.
Ervaring GBS-patiënt: ?En dan maar kijken op de klok, die recht voor me hing. Minuutje na minuutje zie je dan voorbij sluipen, want je hebt niets anders te doen. Dan leef je toe naar ieder bezoekuur. Ger was er gelukkig altijd al om 10.30 uur. En dan bleef hij zo lang mogelijk. Dan ging hij even weg, en was dan meestal om een uur of twee, half drie weer terug tot het eind van de dag. En ?s avonds altijd om 19.30 uur tot zo lang het mocht?. (Bron: www.guillain-barre.nl)
Patiënten met het GBS worden vaak gedurende lange tijd beademd en zullen een tracheostoma krijgen. Echter 25-30 procent van de patiënten wordt korter dan 2-3 weken beademd. Geadviseerd wordt het plaatsen van een tracheostoma uit te stellen tot na deze periode, omdat de kans reëel is dat het niet nodig blijkt te zijn. Als een patiënt langer dan 2-3 weken beademd wordt, zonder tekenen van herstel, dient een tracheostomie te worden overwogen. Soms worden patiënten met het GBS ernstig verlamd zijn intermitterend gesedeerd. Dit dient bij voorkeur in overleg met de patiënt te gebeuren. Goede pijnstilling kan de noodzaak tot sedatie verminderen. In het algemeen moet de Intensive Care patiënt zo min mogelijk gesedeerd zijn, maar sedatie is verdedigbaar bij patiënten die zo ernstig verlamd zijn dat geen enkele vorm van communicatie mogelijk is. Binnenkort komt de CBO richtlijn ?Guillain-Barré syndroom? uit, hierin is meer informatie te vinden over deze onderwerpen.
Aandachtspunten
1. autonome disfunctie; hierdoor kunnen overdreven sterke vagale reacties bij de verzorging ontstaan (bijvoorbeeld hartritmestoornissen);
2. corneabeschadiging als de ogen niet (goed) gesloten kunnen worden;
3. obstipatie/ileus, door immobilisatie en/of autonome disfunctie;
4. pijn: herkenning en bij behandeling regelmatig effectiviteit van de
behandeling nagaan;
5. slikstoornis met dreigende aspiratiepneumonie;
6. trombosebeen/longembolie; profylaxe met nadroparine is nodig
zolang de patiënt het grootste gedeelte van de dag rolstoelafhankelijk/
bedlegerig is;
7. decubitus: wisselligging, anti-decubitus-matras;
8. onrust/angst bij beademde patiënt:
a. bespreek angsten (angst voor uitvallen van de beademingsapparatuur);
b. regelmatig binnenlopen bij patiënt;
c. voorkom over- of onderprikkeling;
d. zorg voor dag-nachtritme;
e. zorg voor aanduiding van tijd en datum binnen gezichtsbereik;
f. ruime bezoekregeling;
g. wees alert op hallucinaties;
h. in overleg met de patiënt kunnen afspraken over sedatie gemaakt worden;
i. overweeg om een groepje vaste verpleegkundigen samen te stellen die de manier van communicatie van de patiënt leren kennen;
9. spierstijfheid,spitsvoeten,contracturen,mobiliseren:fysiotherapie, revalidatiearts
10.verwerkingsproblematiek: contact met ex-Guillain-Barré patiënten via Vereniging Spierziekte Nederland (VSN), ook in de progressieve fase kan de vereniging specifieke informatie verstrekken;
11. communicatie:
a. eenduidige afspraken maken over communicatie (alfabetbord, communicatiekaart, groen/rode kaarten);
b. blijf de patiënt betrekken bij beslissingen;
c. handelingen aankondigen en uitleggen;
d. oogcontact maken alvorens een handeling aan te vangen;
e. niet over de patiënt praten in zijn/haar bijzijn.
Statement
De voorzitter van de CBO werkgroep van de CBO richtlijn ?Guillain- Barré-syndroom?, Prof. Dr. P.A. van Doorn, neuroloog Erasmus MC, heeft commentaar gegeven op deze tekst en aanbevelingen beschreven in deze tekst volgen de CBO richtlijn. Ook Dr. M. van der Jagt, neuroloog-intensivist, Erasmus MC, heeft commentaar gegeven op deze tekst.
Literatuur
1. Guillain G BJ, Strohl A. Sur un synfrome de radiculo-nevrite avec hyperalbuminose du liquide cephalo-rachidien sans reaction cellulaire: Remarques sur les caracteres cliniques et graphiques des reflexes tendineux. Bull Mem Soc Med Hop Paris 1916;40:1462-1470.
2. Koningsveld R van, Doorn PA vcan, Schmitz PI, Ang CW, Meche FG van der. Mild forms of Guillain-Barre syndrome in an epidemiologic survey in The Netherlands. Neurology 2000;8;54(3):620-625.
3. Doorn PA van, Ruts L, Jacobs BC. Clinical features, pathogenesis, and treatment of Guillain-Barre syndrome. Lancet neurology 2008;7(10):939-950.
4. Walgaard C, Lingsma HF, Ruts L, Drenthen J, Koningsveld R van, Garssen MJP, et al. Prediction of respiratory insufficiency in Guillain-Barre syndrome. Annals of neurology 2010.
5. Moulin DE, Hagen N, Feasby TE, Amireh R, Hahn A. Pain in Guillain-Barre syndrome. Neurology 1997;48(2):328-331.
6. Flachenecker P. Autonomic dysfunction in Guillain-Barre syndrome and multiple sclerosis. Journal of neurology 2007;254 Suppl 2:II96-II101.
7. Lawn ND, Wijdicks EF. Fatal Guillain-Barre syndrome. Neurology 1999;52(3):635- 638.
8. Merkies IS, Schmitz PI, Samijn JP, Meche FG van der, Doorn PA van. Fatigue in im- mune-mediated polyneuropathies. European Inflammatory Neuropathy Cause and Treatment (INCAT) Group. Neurology 1999;10;53(8):1648-1654.
9. Vries JM de, Hagemans ML, Bussmann JB, Ploeg AT van der, Doorn PA van. Fatigue in neuromuscular disorders: focus on Guillain-Barre syndrome and Pompe disease. Cell Mol Life Sci 2009;16.
10. Garssen MP, Koningsveld R van, Doorn PA van. Residual fatigue is independent of an- tecedent events and disease severity in Guillain-Barre syndrome. Journal of neurology 2006;253(9):1143-1146.
11. Garssen MP, Bussmann JB, Schmitz PI, Zandbergen A, Welter TG, Merkies IS, et al. Physical training and fatigue, fitness, and quality of life in Guillain-Barre syndrome and CIDP. Neurology 2004;28;63(12):2393-2395.
12. Hughes RA, Swan AV, Raphael JC, Annane D, Koningsveld R van, Doorn PA van. Immunotherapy for Guillain-Barre syndrome: a systematic review. Brain. 2007;130(Pt 9):2245-2257.
13. Dornonville de la Cour C, Andersen H, Stalberg E, Fuglsang-Frederiksen A, Jakobsen J. Electrophysiological signs of permanent axonal loss in a follow-up study of patients with Guillain-Barre syndrome. Muscle & Nerve 2005;31(1):70-77.
14. Bernsen RA, Jager Aede , Schmitz PI, Meche FG van der. Residual physical outcome and daily living 3 to 6 years after Guillain-Barre syndrome. Neurology 1999;22;53(2):409-410.
15. Bernsen RA, Jager AE de, Schmitz PI, Meche FG van der. Long-term impact on work and private life after Guillain-Barre syndrome. Journal of the neurological sciences 2002;15;201(1-2):13-17.
16. Ruts L, Koningsveld R van, Doorn PA van. Distinguishing acute-onset CIDP from Guillain-Barre syndrome with treatment related fluctuations. Neurology 2005;12;65(1):138-140.
17. Hughes RA, Swan AV, Koningsveld R van, Doorn PA van. Corticosteroids for Guillain- Barre syndrome. Cochrane database of systematic reviews (Online). 2006(2):CD001446.
18. Double-blind trial of intravenous methylprednisolone in Guillain-Barre syndrome. Guillain-Barre Syndrome Steroid Trial Group. Lancet 1993 Mar 6;341(8845):586-590.
19. Koningsveld R van, Schmitz PI, Meche FG van der, Visser LH, Meulstee J, Doorn PA van. Effect of methylprednisolone when added to standard treatment with intravenous immunoglobulin for Guillain-Barre syndrome: randomised trial. Lancet 2004;17;363(9404):192-196.
20. Randomised trial of plasma exchange, intravenous immunoglobulin, and combined treatments in Guillain-Barre syndrome. Plasma Exchange/Sandoglobulin Guillain- Barre Syndrome Trial Group. Lancet 1997;25;349(9047):225-230.
21. Jacobs BC, Rothbarth PH, Meche FG van der, Herbrink P, Schmitz PI, Klerk MA de, et al. The spectrum of antecedent infections in Guillain-Barre syndrome: a case-control study. Neurology 1998;51(4):1110-1115.
22. Ang CW, Jacobs BC, Laman JD. The Guillain-Barre syndrome: a true case of molecular mimicry. Trends in immunology 2004;25(2):61-66.