Meld je aan voor onze nieuwsbrief
Bij het aanmelden ga je akkoord met onze Privacy Policy
Inleiding
Wanneer patiënten die behandeld worden met orale anticoagulantia een invasieve ingreep ondergaan moet het antistollingsbeleid tijdelijk worden aangepast. Orale anticoagulantia zijn vitamine K antagonisten (VKA, bijvoorbeeld Sintrommitis of marcoumar), thrombocytenaggregatieremmers (TAR, bijvoorbeeld clopidogrel) of de Nieuwe Orale Anticoagulantia (NOAC) waaronder dabigatran. De aanpassing van het antistollingsbeleid betreft maatwerk waarbij een goede individuele afweging nodig is van enerzijds het trombo-embolie risico bij staken en anderzijds het bloedingsrisico bij het continueren ervan1.
Overbruggingsbehandelingen
Indien het risico op trombo-embolie tijdens de onderbreking van VKA onaanvaardbaar is, kan een overbruggingsbehandeling met heparines worden gekozen. Vaak kan bij kleine ingrepen kan de antistollingsbehandeling worden gecontinueerd. De risico-inschatting en het behandelplan dient bij electieve operatiepatiënten ruim van te voren te worden gemaakt zodat alle betrokken geïnformeerd zijn.
Onder ?bridging of overbruggingsbehandeling? wordt verstaan de toepassing van parenterale, kortwerkende anticoagulantia, Unfractioned Heparin (UFH) of Low Molecular Weight Heparin (LMWH) tijdens onderbreking van de behandeling met orale anticoagulantia rondom een ingreep2-3.
Hoewel niet voor alle indicaties de effectiviteit van LMWH in vergelijking met UFH onomstotelijk is bewezen, wordt geadviseerd LMWH bij overbruggingsbehandeling toe te passen. De veiligheid van LMWH ten opzichte van UFH lijkt voldoende aangetoond4.
In het algemeen geldt dat overbruggingsbehandeling geïndiceerd is bij patiënten met mechanische hartkleppen, doorgemaakte trombose of longembolie < 6 maanden voor de ingreep of andere patiënten met een hoog risico op arteriële en veneuze trombose (zie tabel 1). Bij overige groep patiënten dient een zorgvuldige afweging gemaakt te worden van trombose- en bloedingrisico.
De verschillende middelen
De meest gebruikte antitrombotica zijn trombocytenaggregatieremmers (TAR) en vitamine K-antagonisten (VKA). Ook zijn de Nieuwe of Directe Orale Anticoagulantia (NOAC?s/DOAC?s) in opmars.
Trombocytenaggregatieremmers:
Acetylsalicylzuur/ASA:
De antitrombotische werking berust op acetylering van het enzym cyclo-oxygenase in de trombocyt, waardoor de vorming van het prostaglandine tromboxaan A2 wordt geremd.
Werkingsduur: tot 7?10 dagen na staken behandeling5.
Carbasalaatcalcium:
Werkt op dezelfde wijze als acetylsalicylzuur5.
Clopidogrel
Remt de plaatjesaggregatie die wordt geïnduceerd door adenosinedifosfaat (ADP) en de meeste andere plaatjesagonisten. De binding van ADP aan de bloedplaatjesreceptor wordt selectief, maar irreversibel geremd alsmede de daaruit voortvloeiende ADP-afhankelijke activering van het GPIIb/IIIa-complex. De snelheid van het herstel van een normale bloedplaatjesfunctie komt overeen met de snelheid waarmee bloedplaatjes worden vernieuwd (ca. 7 dagen) 5.
NB:
Dipyridamol/Persantin, is een fosfodiësterase-remmer die een reversibele trombocytenaggregatieremming geeft en een korte halfwaardetijd van 2.2-3 uur heeft5. In de literatuur worden hierover, in het kader van perioperatief antistollingsbeleid, geen uitspraken gedaan. In de praktijk wordt dit adjuvante medicijn 5-7 dagen preoperatief gestopt en bij voorkeur de ASA gecontinueerd.
Vitamine K-antagonisten:
Acenocoumarol en fenprocoumon:
Dit zijn beide vitamine K-antagonisten van de synthese van de stollingsfactoren II, VII, IX en X. Acenocoumarol heeft een halfwaardetijd van 8-12 uur en fenprocoumon van 160 uur, waardoor de acenocoumarol na circa 3 dagen geheel is uitgewerkt en fenprocoumon pas na 7-10 dagen5.
De werking van deze middelen zijn te couperen met vitamine K en Beriplex.
Nieuwe Orale Anticoagulantia6:
De drie momenteel geregistreerde, nieuwe orale anticoagulantia (NOAC?s), zijn de trombineremmer dabigatran (Pradaxa®) en de factor-Xa-remmers apixaban (Eliquis ®) en rivaroxaban (Xarelto ®) voor verschillende indicaties te weten:
Preventie van veneuze trombo-embolie bij volwassen patiënten die electief een heup- of knievervangende operatie ondergaan.
Preventie van een cerebrovasculair accident (CVA) en systemische embolie bij volwassen patiënten met non?valvulair atriumfibrilleren met minimaal één risicofactor zoals congestief hartfalen, hypertensie, leeftijd ? 75 jaar, diabetes mellitus, een eerder CVA of eerdere TIA.
Behandeling van diep?veneuze trombose (DVT) en pulmonale embolie (PE) en preventie van recidief DVT en PE bij volwassen patiënten.
– NB: de indicaties verschillen per middel, zie hiervoor het farmacotherapeutisch kompas.
De voordelen van VKA?s is het frequent monitoren van de INR-waarde door de trombosediensten waarmee onder andere de compliantie beter gevolgd kan worden. Enkele nadelen zijn de noodzaak van regelmatige bloedafnames en dosisaanpassingen in verband met dieet, co-morbiditeit en/of co-medicatie. De behandeling met een NOAC is even effectief of effectiever dan de behandeling met een VKA gebleken in onderzoeken. Daarnaast zou de behandeling met NOAC?s gepaard gaan met minder (ernstige) bloedingscomplicaties in vergelijking tot de behandeling met VKA?s. Grote beperkingen die verbonden zijn aan het gebruik van NOAC?s, zijn het ontbreken van een specifiek antidotum, het vooralsnog ontbreken van specifieke laboratoriumtesten in het ziekenhuis om de werkzaamheid te meten.
Benadering bij preoperatief gebruik van Vitamine K-antagonisten
De beslissing om een operatie te overbruggen met antistollingsbehandeling hangt af van verschillende factoren, waaronder het perioperatieve trombose-risico. Deze wordt bepaald op de anesthesiologische preoperatieve screeningspolikliniek. Het risico wordt onderverdeeld in drie categorieën, te weten: hoog, intermediair en laag7. Zie tabel 1.
Tabel 1: risico op arteriële en veneuze trombo-embolie.
|
Arteriële trombo-embolie |
||
|
|
Jaarlijks risico |
|
|
Hoog |
> 10% |
|
|
Intermediar |
5-10% |
|
|
Laag |
< 5% |
|
|
* De literatuur is niet eenduidig; het tromboserisico varieert van 10-12% tot 5-10% |
||
|
Veneuze trombo-embolie |
||
|
|
1-maandsrisico |
|
|
Hoog |
> 10% |
|
|
Intermediar |
2-10% |
|
|
Laag |
< 2% |
|
Afkortingen: AF= atriumfibrilleren; MHV= mechanic heart valve ofwel mechanische hartklep; CVA= cerebrovasculair accident of beroerte; TIA: transient ischaemic attack; VTE= veneuze trombo-embolie.
Toelichting:
Weergave van het risico op trombose zonder gebruik van vitamine K-antagonisten7. De arteriële trombose wordt ingedeeld in een jaarlijks tromboserisico en de veneuze in een maandelijks. De CHA2DS2-VASc -score wordt gebruikt om het risico op arteriële trombo-embolie bij atriumfibrilleren te bepalen.
|
|
Kenmerk/risicofactoren |
Punten |
|
C H A D S V A Sc |
Congestief hartfalen Hypertensie Leeftijd > 75 Diabetes Mellitus Stroke (eerdere TIA of beroerte) Vasculaire ziekte 65-74 Geslacht vrouw (sex category) |
1 1 2 1 2 1 1 1 |
|
Maximale score |
9 |
|
Bij een CHA2DS2-VASc-score van >4 is er een additioneel risico van meer dan 6% en wordt als hoog risico afgegeven waarbij bridging noodzakelijk is. Indien AF werd gecompliceerd door TIA/CVA wordt ongeacht de score bridging geadviseerd.
Periopereratief beleid gebruik van vitamine K-antagonisten
Vervolgens wordt met behulp van deze inschatting het perioperatieve beleid bepaald. Alleen bij hoog risico op arteriële en/of veneuze trombo-embolie is overbrugging geïndiceerd. Op basis van de literatuur lijkt bij patiënten met een intermediair en laag risico, een overbruggingsschema met een therapeutische dosering LMWH of ongefractioneerde heparine niet zinvol. Daarom is in tabel 2 gekozen voor twee overbruggingsschema?s, waarbij in de perioperatieve periode de groepen met intermediair en laag risico, allebei worden behandeld met een profylactische dosering antistollingsmedicatie. Dit is gedaan aangezien het bloedingsrisico bij therapeutische dosering hoger lijkt dan het trombo-embolische risico.
Tabel 2: overbruggingsstrategieën.
|
Tromboserisico à (toenemend) |
Hoog |
|
Preoperatief – stop behandeling met VKA (acenocoumarol: 3-4 dagen, fenprocoumon: 5-7 dagen) NB: zie toelichting overbruggingtherapieën bij gebruik van VKA. Postoperatief – 12-24* uur postoperatief: herstart VKA-behandeling (tenzij bij actieve bloeding) – 12-24* uur postoperatief: start therapeutisch toediening van LMWH of UFH – stop behandeling met LMWH of UFH indien INR >2.0 (2 maal gemeten op 2 verschillende dagen) * overweeg bij een hoog trombo-embolierisico LMWH/UFH 12 uur na de ingreep te herstarten.
|
|
Laag |
Preoperatief – stop behandeling met VKA (acenocoumarol: 3-4 dagen, fenprocoumon: 5-7 dagen) – op ochtend van operatie: INR bepalen Postoperatief – 12-24 uur postoperatief: herstart VKA-behandeling (tenzij bij actieve bloeding) – Gebruikelijke profylactische LMWH-dosering |
||
|
|
Laag |
Hoog |
|
|
Bloedingsrisico (tijdens operatie) |
|||
Afkortingen: VKA= vitamine K-antagonist; LMWH = laagmoleculaire heparine, UFH= ongefractioneerde heparine, INR= international normalised ratio.
Perioperatieve overbruggingsstrategieën bij patiënten die antistollingsbehandeling gebruiken, zijn afhankelijk van trombose- en bloedingsrisico. Nadat men in tabel 1 het trombo-embolierisico heeft bepaald, kan men in deze tabel kiezen uit 2 schema?s. Hierbij geldt het schema met hoog tromboserisico (boven in deze figuur) voor de hoogrisicogroep uit tabel 1. De groepen met laag en middelmatig risico uit tabel 1 zullen het overbruggingschema krijgen voor laag tromboserisico, zoals hier onderaan weergegeven.
Afkortingen: VKA= vitamine K-antagonist; LMWH = laagmoleculaire heparine, UFH= ongefractioneerde heparine, INR= international normalised ratio.
Overbruggingstherapieën bij gebruik van vitamine K-antagonisten
Ongefractioneerde heparine (UFH)
Start behandeling bij een INR van < 2.0 (VKA is, afhankelijk van het preparaat, al enkele dagen gestopt).
Instelling heparine-behandeling op geleide van de geactiveerde partiële tromboplastinetijd (APTT), met als streefwaarde: 2.0-2.5 maal de uitgangswaarde.
Tijdstip van stoppen en herstarten rondom operatie is belangrijk.
4-6 uur preoperatief stoppen is veilig genoeg om bloedingcomplicaties te voorkomen8.
Bij goede chirurgische hemostase kan de UFH-toediening weer worden hervat. Meestal hanteert men een interval van 24 uur tussen operatie en herstart.
NB: bij verhoogd trombo-embolierisico kan het interval, mits goede hemostase, verkort worden naar 12 uur.
Cave Heparin induced trombocytopenia: dit is een trombocytopenie geïnduceerd door heparine die meestaal meer dan 5 dagen na start van heparinetherapie ontstaat. Het wordt veroorzaakt door heparine-afhankelijke IgG antilichamen tegen complexen van plaatjesfactor 4 (PF4) en heparine, die bloedplaatjes activeren met als resultaat trombinegeneratie en trombotische complicaties. Trombopenie komt vaak voor bij patiënten in het ziekenhuis die heparine krijgen, maar slechts een klein deel hiervan heeft daadwerkelijk een HIT.
Laagmoleculair gewicht heparine (LMWH)
Toepassing van LMWH bij preventie en behandeling van arteriële en veneuze trombo-embolie blijkt minstens zo effectief te zijn als die met UFH en zelfs veiliger dan dit laatste middel.
Voordelen: subcutane toediening, thuisgebruik, voorspelbare farmacokinetiek zodat geen laboratoriumcontrole nodig is (dit geldt minder in het geval van nierfunctiestoornissen, mogelijkheid tot sturing o.b.v. anti-Xa-spiegels of keuze voor UFH bij creatinineklaring van < 30 ml/min)9.
Nadelen: langere halfwaardetijd m.a.g. minder flexibiliteit in de timing van de invasieve ingreep, ontbreken specifiek antidotum.
Algemeen beleid:
Start behandeling bij een INR van < 2.0 (VKA is afhankelijk van het preparaat al enkele dagen gestopt) of op dag ?2 en ?1 preoperatief.
Laatste gift minstens 24 uur preoperatief. Advies is dan ook om bij electieve patiënten de LMWH ?s ochtends toe te dienen, om het risico op bloedingen te reduceren.
Perioperatief beleid bij gebruik van trombocytenaggregatieremmers (TAR)
Patiënten die TAR gebruiken kunnen worden verdeeld in twee groepen:
Primaire preventie (= geen hart- en vaatziekten) en
Secundaire preventie (= status na acuut coronairsyndroom, stent, CVA of bij perifeer vaatlijden).
Vervolgens wordt een risico-inschatting op trombose gemaakt, alwaar een te volgen beleid uit voortkomt:
hoog trombose risico =binnen 6 weken na een acuut coronair syndroom, PCI, plaatsen van een bare metal stent (BMS), CVA of binnen 12 maanden na plaatsen van drug eluting stent (DES) of hoog risico stents.
Laag trombose risico: > 3 maanden na BMS, CVA, ongecompliceerd MI, PCI zonder stenting.
Algemene overwegingen:
Bij een normale trombocytenproductie is na 3-5 dagen de trombocytenaggregatie al voldoende hersteld. Hierdoor volstaat 5 dagen preoperatief stoppen met inname van ascal en/of plavix.
Trombose in een coronaire stent gaat gepaard met een hoge mortaliteit (15%) en morbiditeit10-11.
Trombo-embolierisico na PTCA afhankelijk van:
interval tussen procedure en operatie;
aan- of afwezigheid van een stent en het type stent:
BMS: trombose treedt vooral op in de eerste 2 weken en is na 4 weken zeldzaam. Na 6 weken kan clopidogrel worden gestaakt waar ascal als preventie voor stenttrombose en secundaire preventie bij atherosclerose, i.p. levenslang wordt gecontinueerd.
NB: staken van acetylsalicylzuur mag alleen bij hoog bloedingsrisico.
DES: stenttrombose kan tot jaren na implantatie optreden12. Clopidogrel mag 12 maanden na PTCA worden gestaakt. Als de patiënt in deze periode geopereerd moet worden dan dient er overleg plaats te vinden met de cardioloog.
Overwegingen: stoppen of doorgaan met TAR:
Continueren van 80-100 mg acetylsalicylzuur leidt tot meer peroperatief bloedverlies maar niet tot verhoogde morbiditeit en mortaliteit10.
Uitzonderingen: transurethrale prostatectomieën en craniotomieën geven een mogelijke stijging van de mortaliteit.
Gebruik van de combinatie: acetylsalicylzuur en clopidogrel geeft een toename van peroperatief bloedverlies van 30-50%13-14.
Op grond van deze overwegingen wordt bij patiënten met een stent een perioperatief antistollingsbeleid geadviseerd zoals beschreven in figuur 1.
Figuur 1: advies voor perioperatief beleid bij patiënten die trombocyten-aggregatieremmers gebruiken14.
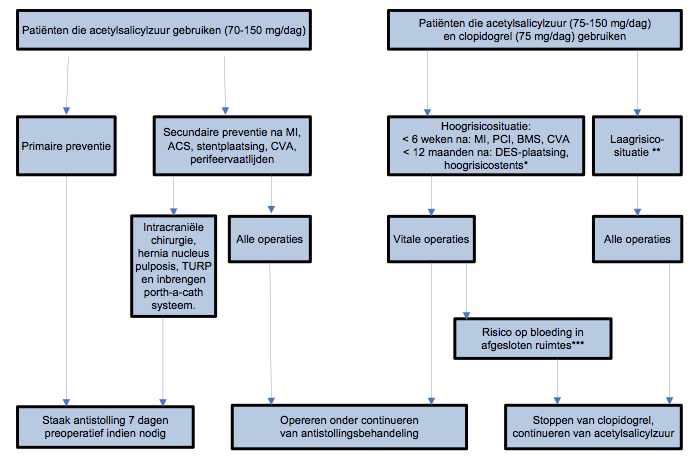
Afkortingen: MI= myocardinfarct; ACS= acuut coronair syndroom; CVA = cerebrovasculair accident (beroerte); PCI= percutane coronaire interventie; BMS= ?bare metal?-stent, DES = ?drug eluting?-stent.
* Als hoogrisicostents gelden: lange (>36 mm), proximale of overlappende stents, multipele stents, stents in chronische totale occlusie, stents in kleine vaten of in bifurcatieafwijkingen
** Voorbeelden van laagrisicosituaties: > 3 maanden na BMS, CVA, ongecompliceerd MI, PCI zonder stenting.
*** Risico op bloeding in gesloten ruimten: intracraniële neurochirurgische ingreep, operatie in het intramedullaire kanaal en een operatie in de achterste oogkamer. In deze situaties moet een risico-batenafweging worden gemaakt van het continueren versus stopen van acetylsalicylzuur per patiënt. Snel postoperatief hervatten van gebruik van acetylsalicylzuur is belangrijk.
NB:
Als in het geval bij stents, stoppen met clopidogrel niet gewenst is moet vanwege de mogelijkheid tot optreden van bloedingen in afgesloten ruimtes, een risico-batenanalyse worden gemaakt. Dit kan in een multidisciplinair overleg met betrokken medisch specialisten zoals cardioloog, snijdend specialist en anesthesioloog. Hieruit volgt het individuele beleid voor de patiënt, die adequaat gedocumenteerd dient te worden.
Theoretisch bestaat ook bij TAR-gebruik de mogelijkheid om te overbruggen, namelijk met tirofiban/Aggrastat®. Dit is een reversibele, selectieve GPIIb/IIIa-receptorantagonist. Het bindt aan glycoproteïne-IIb/IIIa-receptoren op het oppervlak van trombocyten. Het remt de trombocytenaggregatie door de binding van klevende glycoproteïnen zoals fibrinogeen en vonwillebrandfactor aan geactiveerde trombocyten te verhinderen.
Werking: 15?60 minuten na toediening wordt de trombocytenaggregatie aanzienlijk (92?95%) geremd. Werkingsduur: na staken van de infusie herstelt de plaatjesfunctie binnen 8 uur tot normaal.
Benadering bij preoperatief gebruik van NOAC?s/DOAC?s6
Bepaal het bloedingsrisico:
Ingrepen met laag bloedingsrisico: NOAC hoeft niet gestaakt te worden
Tandheelkundige ingrepen (extractie 1-3 tanden of kiezen, operatieve verstandskiesverwijdering, parodontale behandeling, wortelkanaalbehandeling, abcesincisie, implantaten, mondhygieniste)
Kleine dermatologische ingrepen, flebologische te weten endovasculaire ablatie (radiofrequent/laser), kleine ambulante flebectomie vlgs Muller
Cataract en glaucoom operaties indien geen retrobulbaire anesthesie
Iedere andere ingreep waarbij goede lokale hemostase mogelijk is.
Ingrepen met standaard bloedingsrisico: NOAC tijdelijk staken
Hartcatheterisatie
Ritme-ablaties
Flebecetomie groot ambulant volgens Muller
Colonoscopie zonder verwijdering van grote poliepen
Ongecompliceerde laparoscopische procedures (bv. cholecystectomie)
PEG plaatsing
Radiologische puncties en/of stenting met goede hemostase mogelijkheid
PTA met/zonder stentplaatsing
Vaatchirurgie met beperkt weefseltrauma (bv. Shuntoperaties, liesarteriedesobstructie)
Ingrepen met een hoog bloedingsrisico: NOAC tijdelijk staken
Hartchirurgie (inclusief pericardiale ingrepen)
Inbrengen van pacemaker of ICDs
Neurochirurgische ingrepen (intracerebraal, intraspinaal, epiduraal)
Grote herniaoperaties
Grote buikchirurgie
Chirurgie met uitgebreide weefselbeschadiging (maligniteit, gewrichtsartroplastiek, plastischereconstructies)
Grote urologische ingrepen
Vaatchirurgische met veel weefseltrauma, retroperitoneaal vaatchirurigie, abdominale vaatchirurgie
Colonoscopie met verwijdering grote poliepen
ERCP met papillotomie
GE diltataties (colon/oesophagus/duodenum)
Radiologische puncties en/of stenting zonder goede hemostase mogelijkheid
Schildklieroperaties
Bepaal type operatie: electief of acuut?
Bepaal vervolgens per medicijn het beleid
Rivaroxaban
Acute operaties (binnen 2 uur)
Bepaal PT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname rivaroxaban
Indien inname < 2 uur en/of PT verlengd: overweeg Beriplex®, recombinant factor VIIa
Als trombocyten < 50 x 109/L geef trombocytentransfusie
Semi-acute operaties (2-12 uur)
Bepaal PT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname rivaroxaban
Indien mogelijk stel operatie uit tot PT genormaliseerd is of (afhankelijk van nierfunctie) één halfwaardetijd is verstreken (normaal is 12 uur, zie ook verder in tabel 2)
Electieve operaties
Dit is afhankelijk van het operatieve bloedingrisico. Indien een volledig normale stolling nodig is kan de PT preoperatief worden bepaald. Bij een normale PT uitslag is het antistollend effect van apixaban (vrijwel) afwezig (NB. tenzij apixaban < 2 uur daarvoor is ingenomen)
Onderbreken rivaroxaban voorafgaand aan operatieve ingreep
|
GFR (ml/min) |
Halfwaardetijd (uren) |
Tijdstip van laatste dosering vóór ingreep Laag bloedingsrisico ? Middel/ hoog bloedingsrisico |
|
|
> 30 |
12 (11-13) |
24 uur |
48 uur (4*T1/2)
|
Overbruggingstherapie
Door de korte halfwaarde van rivaroxaban is overbruggingstherapie (met LMWH) over het algemeen niet nodig. Bij hoog trombo-embolisch risico moet overwogen worden sneller te herstarten met rivaroxaban na de operatie (zie volgend kader).
Rivaroxaban herstart na (electieve) operatie
Herstart als complete hemostase. Aangezien rivaroxaban al na 2 uur therapeutisch antistollend is, is het advies bij een standaard bloedingrisico 24-48 uur na de operatie te herstarten met rivaroxaban. Bij een hoog bloedingsrisico 48-72 uur na de operatie starten. Bij een patiënt met een hoog trombo(-embolie)risico (bv. bij CHA2DS2-VASc score ? 4 bij patiënt met boezemfibrilleren of diep veneuze thrombose in de afgelopen 4 weken) moet overwogen worden bij goede hemostase rivaroxaban te starten op de avond van de dag van de ingreep. Daarnaast kan bij recente DVT een vena kava filter overwogen worden.
Dabigatran
Acute operaties (binnen 2 uur)
Bepaal aPTT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname dabigatran.
Indien inname < 2 uur en/of aPTT verlengd: overweeg Beriplex®, recombinant factor VIIa.
Als trombocyten < 50 x 109/L geef trombocytentransfusie.
Semi-acute operaties (2-12 uur)
Bepaal aPTT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname dabigatran.
Indien mogelijk stel operatie uit tot aPTT genormaliseerd is of (afhankelijk van nierfunctie) één halfwaardetijd is verstreken (normaal is 12 uur, zie ook verder in tabel 2)
Electieve operaties
Dit is afhankelijk van het operatieve bloedingrisico. Indien een volledig normale stolling nodig is kan de aPTT pre-operatief worden bepaald. Bij een normale aPTT uitslag is het antistollend effect van dabigatran (vrijwel) afwezig (NB. tenzij dabigatran < 2 uur daarvoor is ingenomen).
Onderbreken dabigatran voorafgaan aan operatieve ingreep
|
eGFR (ml/min) |
Halfwaardetijd (uren) |
Tijdstip van laatste dosis voor ingreep: Standaard bloedingsrisico ? Hoog bloedingsrisico |
|
|
> 50 |
13 (11-22) |
24 uur |
48 uur |
|
30-50 |
18 (13-23) |
48 uur |
72 uur |
Overbruggingstherapie
Door de korte halfwaarde van dabigatran is overbruggingstherapie (met LMWH) over het algemeen niet nodig. Bij hoog trombo-embolisch risico moet overwogen worden sneller te herstarten met dabigatran na de operatie.
Dabigatran herstart na (electieve) operatie
Herstart pas bij complete hemostase. Aangezien dabigatran al na 2 uur therapeutisch antistollend is, is het advies bij een standaard bloedingrisico 24-48 uur na de operatie te herstarten met dabigatran. Bij een hoog bloedingsrisico pas na 48-72 uur na de operatie starten. Bij een patiënt met een hoog trombo(-embolie)risico (bv. bij CHA2DS2-VASc score ? 4 bij patiënt met boezemfibrilleren of diep veneuze thrombose in de afgelopen 4 weken) moet overwogen worden bij goede hemostase dabigatran te starten op de avond van de dag van de ingreep.Daarnaast kan bij recente DVT een vena cava filter overwogen worden.
Apixaban
Acute operaties (binnen 2 uur)
Bepaal PT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname apixaban
Indien inname < 2 uur en/of PT verlengd: overweeg Beriplex®, recombinant factor VIIa
Als trombocyten < 50 x 109/L geef trombocytentransfusie
Semi-acute operaties (2-12 uur)
Bepaal PT, kreatinine, Trombocyten, Hb.
Bepaal tijdstip laatste inname apixaban
Indien mogelijk stel operatie uit tot PT genormaliseerd is of (afhankelijk van nierfunctie) één halfwaardetijd is verstreken (normaal is 12 uur, zie ook verder in tabel 2)
Electieve operaties
Dit is afhankelijk van het operatieve bloedingrisico. Indien een volledig normale stolling nodig is kan de PT preoperatief worden bepaald. Bij een normale PT uitslag is het antistollend effect van apixaban (vrijwel) afwezig (NB. tenzij apixaban < 2 uur daarvoor is ingenomen)
Ingrepen met laag bloedingsrisico: apixaban hoeft niet gestaakt te worden
Tandheelkundige ingrepen (extractie 1-3 tanden of kiezen, operatieve verstandskiesverwijdering, parodontale behandeling, wortelkanaalbehandeling, abcesincisie, implantaten, mondhygieniste)
Kleine dermatologische ingrepen, flebologische te weten endovasculaire ablatie (radiofrequent/laser), kleine ambulante flebectomie vlgs Muller.
Cataract en glaucoom operaties indien geen retrobulbaire anesthesie
Iedere andere ingreep waarbij goede lokale hemostase mogelijk is
Onderbreken apixaban voorafgaand aan operatieve ingreep
|
GFR (ml/min) |
Halfwaardetijd (uren) |
Tijdstip van laatste dosering vóór ingreep Laag bloedingsrisico ? Middel/ hoog bloedingsrisico |
|
|
> 30 |
12 (8-15) |
24 uur |
48 uur (4*T1/2)
|
Overbruggingstherapie
Door de korte halfwaarde van apixaban is overbruggingstherapie (met LMWH) over het algemeen niet nodig. Bij hoog thrombo-embolisch risico moet overwogen worden sneller te herstarten met apixaban na de operatie (zie volgend kader).
Apixaban herstart na (electieve) operatie
Herstart als complete hemostase. Aangezien apixaban al na 2 uur therapeutisch antistollend is, is het advies bij een standaard bloedingrisico 24-48 uur na de operatie te herstarten met apixaban. Bij een hoog bloedingsrisico 48-72 uur na de operatie starten. Bij een patient met een hoog thrombo(-embolie)risico (bv. bij CHA2DS2-VASc score ? 4 bij patiënt met boezemfibrilleren of diep veneuze thrombose in de afgelopen 4 weken) moet overwogen worden bij goede hemostase apixaban te starten op de avond van de dag van de ingreep. Daarnaast kan bij recente DVT een vena kava filter overwogen worden.
Literatuurlijst
- Jong J.S, Vink R, et al. Perioperatieve onderbreking van antistollingsmiddelen, stand van zaken, praktische aanbevelingen. Nederlands Tijdschrift voor Geneeskunde. 2009;153:A83
- Dunn AS, Wisnivesky J, Ho W, Moore C, McGinn T, Sacks JS. Perioperative managemnent of patient on oral anticoagulants: a decision analysis. Med Decis Making. 2005;25:387-97
- Kearon C, Hirsch J. Managing of anticoagulation before and after surgery in patients who require oral anticoagulants. New Englang Journal of Medicine. 1997;336:1506-11
- Douketis, ?LMWH as bridging anticoagulation during interruption of warfarin?; Arch of Intern Med 2004
- Farmacotherapeutisch kompas: prepataatteksten bij clopidogrel en acetylsalicylzuur. Diemen, college voor zorgverzekeringen; 2010.
- Leidraad Begeleide introductie Nieuwe Orale Anticoagulantia, werkgroep wetenschappelijke verenigingen en de Orde van Medisch Specialisten.
- Kwaliteitsinstituut voor de gezondheidszorg CBO. Richtlijn Diagnostiek preventie en behandeling van veneuze trombo-embolie en secundaire preventie arteriële trombose. Alphen aan den Rijn: Van Zuiden Communications; 2008
- Vink R, van Dongen CJ, Jacobs R, et al.Thromboembolic and bleeding complications duringnon-cardiac surgery in patients with mechanical heart valves. Journal of Thrombosis and Haemostasis 2005;(Suppl 1): abstract po421.
- Lim W, Low-molecular-weight heparin in patients with chronic renal insufficiency. Internal and Emergency Medicine.
- Burger W, Chemnitius JM, Kneissl GD, Rücker G. Low-dose aspirin for secondary prevention ? cardiovascular risks agter its perioperative withdrawal versus bleeding risks with its continuation. Journal of Internal Medicine. 2005;257:399-414.
- Ong AT, Hoye A, Aoki J, van Mieghem CA, Rodriguez Granillo GA, Sonnenschein K, et al. Thirty-day incidence and six-month outcome of thrombotic stent occlusion after bare-metal, sirolimus, or paclitaxel stent implantation. Journal of the American College of Cardiology. 2005;45:947-53.
- Capodanno D, Capodanno P, Bucalo R, Sanfilippo A, Ruperto C, Caggegi A, et al. A novel approach to define risk of stent thrombisis after percutaneous coronary intervention with drug-eluting stents: the DERIVATION-score. Clinical research in Cardiology. 2009;98:240-8.
- Eikelboom JW, Hirsh J. Bleeding and management of bleeding. European Heart Journal. 2006;8:G38-45.
- Chassot PG, Delabays A, Spahn DR. Perioperative antplatelet therapy: the casefor continuing therapy in patients at risk of myocardial infarctation. Britisch Journal of Anaesthesiology. 2007;99:316-328.